Гейтлера
Cтраница 1
Гейтлера и ( Германия), содержащая квантово-механический молекул водорода. При построении волновой электронов такой молекулы они вначале предположили, состояние электронов в молекуле не должно сильно от их состояния в составляющих молекулу атомах. [1]
Гейтлера - Лондона) для обоснования химической теории валентности, заключающаяся в следующем: для осуществления одной химической связи необходимо, чтобы в двух сближенных атомах имелись два электрона с противоположно ориентированными спинами и чтобы волновые функции их перекрывались; Для двойной химической связи требуются две пары электронов с противоположно ориентированными спинами. [2]
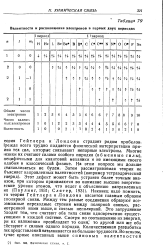 |
Валентности и расположение электронов в первых двух периодах. [3] |
Гейтлера и Лондона страдает рядом пробелов, [ режде всего трудно поддается физической интерпретации при-ина тех сил, которые связывают непарные электроны. Многие шзики их считают силами особого порядка ( обменные сил ы), пецифичными для квантовой механики и не имеющими своего одобия в классической физике. [4]
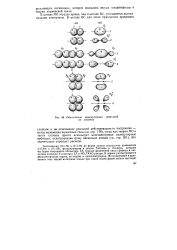 |
Образование молекулярных орбиталей из атомных. [5] |
Гейтлера и Лондона, которую мы будем сокращенно обозначать ГЛ. [6]
Гейтлера - Лондона, может образовать связь с атомом водорода. [7]
Гейтлера и Лондона и, следовательно, насыщаемости ковалентной связи сводится: к тому, что присоединение третьего атома водорода к молекуле Н2 невозможно, так как его спин будет обязательно совпадать со спином одного из двух электронов молекулы. Поэтому между третьим атомом водорода и Н2 будут действовать силы отталкивания, в результате никакого перекрывания электронных облаков не может быть. [8]
Приведенная у Гейтлера ( [1], стр. [9]
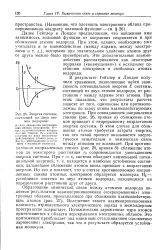 |
Энергия системы, состоящей из двух атомов водорода. [10] |
В результате Гейтлер и Лондон получили уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния г между ядрами этих атомов. При этом оказалось, что результаты расчета зависят от того, одинаковы или противоположны по знаку спины взаимодействующих электронов. При совпадающем направлении спинов ( рис. 26, кривая а) сближение атомов приводит к непрерывному возрастанию энергии системы. В этом случае для сближения атомов требуется затрата энергии, так что такой процесс оказывается энергетически невыгодным и химическая связь между атомами не возникает. При противоположно направленных спинах ( рис. 26, кривая б) сближение атомов до некоторого расстояния г0 сопровождается уменьшением энергии системы. Но это и означает, что в случае противоположно направленных спинов атомных электронов образуется молекула Н2 - устойчивая система из двух атомов водорода, находящихся на определенном расстоянии друг от друга. [11]
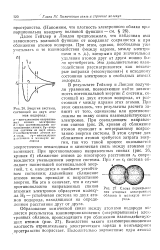 |
Энергия системы, состоящей из двух атомов водорода.| С. ма перекрывания атомных электронных. [12] |
В результате Гейтлер и Лондон получили уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния г между ядрами этих атомов. При этом оказалось, что результаты расчета зависят от того, одинаковы или противоположны по знаку спины взаимодействующих электронов. При совпадающем направлении спинов ( рис. 26, кривая а) сближение атомов приводит к непрерывному возрастанию энергии системы. В этом случае для сближения атомов требуется затрата энергии, так что такой процесс оказывается энергетически невыгодным и химическая связь между атомами не возникает. При противоположно направленных спинах ( рис. 26, кривая б) сближение атомов до некоторого расстояния г0 сопровождается уменьшением энергии системы. [13]
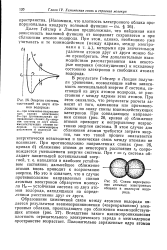 |
Энергия системы, состоящей из двух атомов водорода. [14] |
В результате Гейтлер и Лондон получили уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния г между ядрами этих атомов. При этом оказалось, что результаты расчета зависят от того, одинаковы или противоположны по знаку спины взаимодействующих электронов При совпадающем направлении спинов ( рис. 26, кривая а) сближение атомов приводит к непрерывному возрастанию энергии системы. В этом случае для сближения атомов требуется затрата энергии, так что такой процесс оказывается энергетически невыгодным и химическая связь между атомами не возникает. При противоположно направленных спинах ( рис. 26, кривая б) сближение атомов до некоторого расстояния г0 сопровождается уменьшением энергии системы. Но это и означает, что в случае противоположно направленных спинов атомных электронов образуется молеку-ла Нг - устойчивая система из двух это-мов водорода, находящихся на опреде-ленном расстоянии друг от друга. [15]
Страницы: 1 2 3