Гейтлера
Cтраница 2
В результате Гейтлер и Лондон получили уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния г между ядрами этих атомов. При этом оказалось, что результаты расчета зависят оттого, одинаковы или противоположны по знаку спины взаимодействующих электронов. [16]
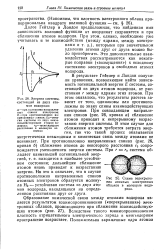 |
Энергия системы, состоящей из двух атомов водорода. [17] |
В результате Гейтлер и Лондон получили уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния г между ядрами этих атомов. При этом оказалось, что результаты расчета зависят от того, одинаковы или противоположны по знаку спины взаимодействующих электронов. При совпадающем направлении спинов ( рис. 26, кривая а) сближение атомов приводит к непрерывному возрастанию энергии системы. В этом случае для сближения атомов требуется затрата энергии, так что такой процесс оказывается энергетически невыгодным и химическая связь между атомами не возникает. При противоположно направленных спинах ( рис. 26, кривая б) сближение атомов до некоторого расстояния гй сопровождается уменьшением энергии системы. Но это и означает, что в случае противоположно направленных спинов атомных электронов образуется молекула На - устойчивая система из двух атомов водорода, находящихся на определенном расстоянии друг от друга. [18]
 |
Длины и энергии связей для Н2 и Н2. [19] |
В сущности, в простой ( Гейтлера - Лондона) теории валентных связей предполагается, что эти структуры несущественны, так как взаимное отталкивание электронов уменьшает вероятность того, что они могут одновременно находиться вблизи одного ядра. Ясно, что оба метода можно улучшить, поскольку каждый описывает некоторые предельные условия. Можно показать, что по мере усовершенствования обоих методов онл сходятся и, наконец, становятся эквивалентными. Модификация методов предусматривает рассмотрение более сложных вол новых функций при соответствующем увеличении трудоемкости вычислений. [20]
 |
Кривая энергии устойчивой молекулы ( / и системы из двух атомов, между которыми не образуется химическая связь ( 2.| Расстояние между частицами в молекуле водорода. [21] |
При построении волновой функции электронов молекулы водорода Гейтлер и Лондон взяли за основу волновую функцию электрона в атоме водорода, находящемся в нормальном состоянии - в ls - сострянии. [22]
 |
Кривая энергии устойчивой молекулы ( / и системы из двух атомов, между кото-рыми не образуется химическая связь ( 2.| Расстояние между частицами в молекуле водорода. [23] |
При построении волновой функции электронов молекулы водорода Гейтлер и Лондон взяли за основу волновую функцию электрона в атоме водорода, находящемся в нормальном состоянии - в ls - состоянии. [24]
 |
Потенциальная энергия системы из двух атомов водорода. 1 - антипарчллельные. 2 - параллельные спины электронов. [25] |
Образование химической связи между атомами водорода в Н2 по Гейтлеру и Лондону обусловлено, таким образом, тем, что движение электронов с антипараллельными спинами около обоих ядер ( а и Ь) приводит к перекрыванию ( взаимопроникновению) электронных облаков и росту плотности электронного облака ( 4я2) в межъядерном пространстве, образованию связывающей орбитали. В случае электронов с параллельными спинами плотность электронного облака ( XF) между ядрами атомов снижается до нуля, так как электроны с параллельными спинами не могут занять общую орбиталь и образования химической связи не происходит. На рис. 5.2 вероятности нахождения электронов для обоих состояний представлены в форме контурных линий, которым соответствует одинаковая электронная плотность. [26]
Принятый в настоящее время метод вывода этих уравнений принадлежит в основном Гейтлеру [24], который, подобно Ми в его теории жидкостей, ограничился рассмотрением структуры решетки типа каменной соли. Как уже подчеркивалось, первоначально эти уравнения относились к молекулам одинаковых размеров, образующих растворы без изменения объема, однако возможно, что в общей форме их можно применять и к другим системам. [27]
Химическая связь, как показали в свое время на примере молекулы водорода Гейтлер и Лондон, образуется за счет увеличения ( по сравнению с невзаимодействующими атомами водорода, находящимися на том же расстоянии, что и в молекуле) электронной плотности между атомами. Это увеличение в расчетах по методу МО учитывается с помощью так называемых интегралов перекрывания. Электроны в основном состоянии молекулы занимают орбитали с наинизшей энергией. На каждой орбитали может находиться по два электрона с противоположными спинами. Здесь к этой общеизвестной школьной модели добавляется одна тонкость. Вследствие электростатического взаимодействия электроны отталкиваются, в результате чего даже два электрона, находящиеся на одной и той же молекулярной орбитали, имеют тенденцию двигаться по возможности на большем удалении друг от друга. Решение уравнения Шредингера для атома водорода облегчается тем, что единственный электрон is этого атома обладает сферической симметрией. В атоме гелия атомная орбиталь вследствие взаимного отталкивания двух электронов Is2 уже не обладает сферической симметрией, и с этим связаны трудности в расчетах распределения электронной плотности в атоме гелия. Энергия корреляции движения электронов может достигать примерно 20 % общей электронной энергии молекулы и в расчетах учитывается с помощью интегралов электронного отталкивания. Кроме того, в молекуле существует еще конфигурационное взаимодействие - взаимодействие между самими молекулярными орбиталями. Волновая функция, учитывающая конфигурационное взаимодействие, аналогична по своей записи уравнению для волновой функции, приведенному в § 1 этой главы, однако вместо ср; волновых функций атомных орбиталей в ее выражение входят Ф - - волновые функции атомных или молекулярных конфигураций. Поясним это понятие на простом примере атома лития, имеющего три электрона. [28]
Химическая связь, как показали в свое время на примере молекулы водорода Гейтлер и Лондон, образуется за счет увеличения ( по сравнению с невзаимодействующими атомами водорода, находящимися на том же расстоянии, что и в молекуле) электронной нлотности между атомами. Это увеличение в расчетах по методу МО учитывается с помощью так называемых интегралов перекрывания. Электроны в основном состоянии молекулы занимают орбитали с наинизшей энергией. На каждой орбитали может находиться по два электрона с противоположными спинами. Здесь к этой общеизвестной школьной модели добавляется одна тонкость. Вследствие электростатического взаимодействия электроны отталкиваются, в результате чего даже два электрона, находящиеся на одной и той же молекулярной орбитали, имеют тенденцию двигаться по возможности на большем удалении друг от друга. Решение уравнения Шредингера для атома водорода облегчается тем, что единственный электрон Is этого атома обладает сферической симметрией. В атоме гелия атомная орбиталь вследствие взаимного отталкивания двух электронов 1 а уже не обладает сферической симметрией, и с этим связаны трудности в расчетах распределения электронной плотности в атоме гелия. Энергия корреляции движения электронов может достигать примерно 20 % общей электронной анергии молекулы и в расчетах учитывается с помощью интегралов электронного отталкивания. Кроме того, в молекуле существует еще конфигурационное взаимодействие - взаимодей - Ътвие между самими молекулярными орбиталями. Волновая функция, учитывающая конфигурационное взаимодействие, аналогична по своей записи уравнению для волновой функции, приведенному в § 1 этой главы, однако вместо pt - волновых функций атомных орбиталей в ее выражение входят Ф - волновые функции атомных или молекулярных конфигураций. Поясним это понятие на простом примере атома лития, имеющего три электрона. [29]
Впервые с позиций квантовой механики природу сил в молекуле водорода объяснили в 1927 г. английские ученые Гейтлер и Лондон. [30]
Страницы: 1 2 3