Плоский ион
Cтраница 1
Плоские ионы или молекулы, в которых существует резонанс между двойными и простыми связями ( например, ацетат-ион и ароматические ядра), проявляют магнитную анизотропность, противоположную по знаку анизотропности оптического двупреломления, причем магнитное двупре-ломление положительно. [1]
Отметим отсутствие плоских ионов SiO32 - и РО3 -; как известно, ионы метасилнката и метафосфата основаны на тетраэдрических группировках SiO4 и РО4 соответственно. Выше уже отмечалось, что аналогичное предпочтение более высоких КЧ характерно и для метаборатов. Все эти молекулы плоские. [2]
Поскольку реакция протекает с образованием плоского иона карбе-ния, то в случае хирального галогеналкана RR R CX должна наблюдаться рацемизация. Это предполагает, однако, достаточно большое время жизни иона карбения, поскольку в противном случае из-за экранирования одной стороны сольватированным уходящим галогенид-ионом атака нуклеофила более вероятна с противоположной стороны, и обращение конфигурации преобладает над ее сохранением. [3]
Согласно этой модели, электрод представляет собой гигантский плоский ион, сольватированный молекулами растворителя. Толщина сольватационного слоя обычно принимается равной диаметру молекул растворителя, ориентированных в соответствии с зарядом электрода. Далее, по представлениям Гельмгольца, располагаются ионы с противоположными знаку электрода зарядами, причем они отделены от сольватационного слоя собственными сольватными оболочками. Плоскость, проведенная через центры ионов, которые под воздействием электростатических сил оказались на расстоянии максимального приближения к поверхности электрода, называется плоскостью Гельмгольца, а область между этой плоскостью и поверхностью электрода - слоем Гельмгольца или плотной частью двойного электрического слоя. [4]
Третья молекула этилендиамина может быть связана с плоским ионом диэтилендиаминмеди ( II) только одной из своих аминогрупп ( так же, как это, по стерическим причинам, может быть в случае этилендиаминового комплекса серебра, см. стр. Но если учесть все обстоятельства, то более вероятно, что комплекс триэтилендиаминмеди ( II) построен окта-едрически. Другими словами, естественнее всего принять, что третья молекула этилендиамина присоединяется через малые равновесные концентрации чис - Диакв Диэтилендиамин-комп-лекса. [5]
Нуклеофил Y - может с одинаковой вероятностью атаковать плоский ион карбония с любой стороны. [6]
Исследование структуры кристаллического дигндрата последнего соединения подтверждает наличие плоских ионов АиВгГ, а в кристаллах Cs AuIAuIIIClt. [7]
Раман-спектре для молекулы, содержащей четырнадцать атомов, в геометрически правильном плоском ионе тропилия активными остаются, теоретически, только четыре полосы в инфракрасной области и семь в Раман-спектре. [8]
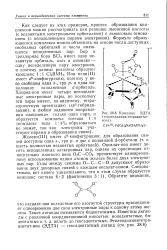 |
Комплекс ЭДТА. [9] |
Оксалат-ион имеет десять неподеленных электронных пар, однако их ориентация относительно плоского иона С С - СО2 препятствует одновременному использованию одним атомом железа более двух электронных пар. Углы между связями О-С - С-О допускают образование двух донорных связей с каждым оксалат-ионом. [10]
В плане общей концепции карбокатионов остается лишь сожалеть, что для трехвалентных плоских ионов типа СН3 стало общеупотребительным название карбониевые ионы. Если это название рассматривать по аналогии с другими ониевыми ионами ( аммониевым, сульфониевым, фосфониевым), то оно должно относиться к более высокому валентному состоянию карбокатиона. Однако очевидно, что карбокатионы в своем наивысшем валентном состоянии являются не трехвалентными, а пентакоординированными катионами типа CHs - Отметим также, что термин карбениевый ион для трехвалентных катионов часто используется в немецкой и французской литературе. Если рассматривать эти ионы как протонирован-ные карбены, то данное название, несомненно, корректно [5] и мы можем легко разграничить карбениевые ( трехвалентные) и карбониевые ( пента - и тетракоординированные) ионы. Следует подчеркнуть, однако, что термин карбениевый ион необходимо употреблять только для трехвалентных ионов, а не в качестве общего наименования всех карбокатионов. [11]
В табл. 4 приведены данные для ионофоров, в составе которых имеется хотя бы один плоский ион. Радиус плоского иона произвольно принят за самый длинный вандерваальсов радиус, идущий от центра тяжести иона. За исключением перхлората трифенилкарбония, это допущение обычно приводит к суммам радиусов, превышающих величины аь. Если предположить, что величина аь действительно является мерой среднего разделения заряда противоположно заряженных ионов при их соприкосновении, то станет ясно, что плоские ионы стремятся ориентироваться таким образом, чтобы взаимодействовать со своим противоположно заряженным ионом наиболее благоприятным способом. В случае метилпиридинийиодида образование комплекса с переносом заряда [44] может уменьшать / Сдисс и &, но, учитывая, что перхлорат проявляет подобное же стремление к ассоциации, этот фактор должен играть незначительную роль. Действительно, молекулы растворителя образуют комплекс преимущественно с иодидом. [12]
Важным моментом в химии трехцентровых карбкатионов яв ляется возможность объяснения стереоспецифичности различных перегруппировок, что исключается в схемах с классическим три-гональным плоским ионом карбония, в котором присоединение мигрирующей алкильной группы равновероятно с обеих сторон атома углерода, несущего заряд. Напротив, в трехцентровом ионе карбония заряженный атом углерода сохраняет свою тетраэдри-ческую конфигурацию, и атака мигрирующей группой может иметь место только со строго определенной стороны данного тетраэдра. [13]
На основании того что три олефина образуют цис - и mpawc - изомеры 1 2-диметил - 1-бром-циклогексана в различных соотношениях, классический плоский ион карбония, как единственный промежуточный ион, исключается. Если классический ион карбония является единственным промежуточным состоянием, то все три олефина должны давать одни и те же продукты, так как образующиеся из них ионы карбония должны быть одинаковы. [14]
В этом случае принять определенную величину для радиуса невозможно, если многоатомный ион очень асимметричен ( как линейный ион азида Щ или плоский ион карбоната СОз -) - Здесь большую роль в определении структуры играют чисто геометрические факторы, сходные с теми, которые были рассмотрены в разделе 11.2 для молекулярных кристаллов. Не удивительно, что возможно очень большое разнообразие кристаллических форм. Имеются, однако, и другие ионы ( например, тетраэдрические ионы NH4 и SO) - при которых результирующее электрическое поле вне молекулы почти не отличается от поля точечного заряда. Например, радиус иона аммония 1 48 А приблизительно равен радиусу иона рубидия, и соли этих двух веществ часто бывают изоморфны. Кристаллы хлористого, бромистого и йодистого аммония при температурах выше соответственно 184, 138 и - 18 С имеют ту же структуру типа NaCl, что и соответствующие галогениды рубидия. Интересно, однако, что при температурах ниже указанных точек происходит превращение их структур в структуру типа CsCl, что иллюстрирует чувствительность структуры к небольшому изменению температуры. [15]
Страницы: 1 2 3