Внешнесферный ион
Cтраница 3
Уменьшение диамагнетизма связано с увеличением во внутренней сфере электроотрицательных групп ( Cl -, NOjf, NOF) - Авторы доказывают это расчетным путем. В основу кладется положение, доказанное авторами на комплексных соединениях платины [73], что диамагнитная восприимчивость ( ДВ) комплексных соединений может быть представлена в виде суммы ДВ отдельных связей кобальта с внутрисферными заместителями и ДВ внешнесферных ионов. [31]
Авторы доказывают это расчетным путем. В основу кладется положение, доказанное авторами на комплексных соединениях платины [73], что диамагнитная восприимчивость ( ДВ) комплексных соединений может быть представлена в виде суммы ДВ отдельных связей кобальта с внутрисферными заместителями и ДВ внешнесферных ионов. [32]
Термин хелат ( chelate - клешневидный) предложен в 1920 г. Морганом и Дрю. Хелаты, в отличие от ВКС, могут быть комплексами катионного, анионного типа или комплексами-неэлектролитами, содержать во внутренней координационной сфере или только полидентатные, или одновременно один или несколько полиден-татных и монодентатные лиганды и иметь или не иметь внешнесферные ионы. Различие между ВКС и ХКС иногда ( но не всегда) не делается: любые ХКС, содержащие хотя бы один хелатный цикл, нередко называют ВКС. В ХКС один и тот же полидентатный лиганд образует один или несколько хелатных циклов, причем этот лиганд может быть би -, 1ри -, тетра -, пента -, гексадентатным. [33]
Среди галидов и оксидов найдены двух -, трех - и шестиядерные кластеры. Шесть атомов молибдена находятся в центрах граней куба, образуя октаэдр Мов; восемь атомов хлора расположены в вершинах куба, каждый атом С1 связан с тремя атомами Мо. Внешнесферные ионы С1 - выполняют роль мостиков, объединяющих кластеры [ Мо6С18 ] между собой. [34]
Среди галидов и оксидов найдены двух -, трех - и шестиядерные кластеры. Шесть атомов молибдена находятся в центрах граней куба, образуя октаэдр Мо6; восемь атомов хлора расположены в вершинах куба, каждый атом С1 связан с тремя атомами Мо. Внешнесферные ионы С1 - выполняют роль мостиков, объединяющих кластеры [ Мо6С18 ] 4 1 между собой. [35]
 |
Структура октаэдрических кластеров типа МвХ8 ( на примере иона Мо6С1 и типа МвХ12 ( на примере иона NbjCliJ. [36] |
По данным рентгеноструктурного анализа, МоС12 отвечает формула [ МовС18 ] СЦ. Об этом же свидетельствуют химические свойства соединения. Внешнесферные ионы С1 - выполняют роль мостиков, объединяющих кластеры [ МовС18 ] 4 между собой. [37]
Затем называют центральный атом. Если валентность центрального атома равна I, то после его названия ставят окончание а; если валентность равна II, то - о; III - ; IV - е; V - ан; VI - он; VII - ин и, наконец, если валентность центрального атома равна VIII, то окончание ен. Только после этого указывают названия внешнесферных ионов. Так, соединение, содержащее комплексный катион [ Со ( ЫНз) е ] С1з, называется гексам-минкобальтихлорид. [38]
Как и в солях, внешнесферные ионы и координационные сферы связаны в кристаллах электростатическими силами. При растворении кристаллического комплексного соединения в воде его кристаллическая решетка разрушается, а координационная сфера и внешнесферные ионы гидратируются. Этот процесс протекает по механизму диссоциации сильных электролитов. Например, K4 [ Fe ( CN) 6 ] и [ А1 ( Н2О) 6 ] С13 представляют собой хорошо растворимые в воде кристаллы. [39]
В этом соединении соседствуют протоны и ионы гидроксила, но реакции нейтрализации не происходит - настолько прочно связывает Pt ( IV) лиганды - ионы ОН -, находящиеся во внутренней координационной сфере. Здесь важнее всего не термодинамическая, а кинетическая устойчивость соединений платины. Даже термодинамически устойчивый, но кинетически лабильный комплекс состава Н2 [ М1у ( ОН) б ] не мог бы существовать сколько-нибудь продолжительное время из-за обмена ионов ОН - на молекулы воды из маточного раствора и сдвига равновесия диссоциации комплекса вследствие нейтрализации протонов внешнесферными ионами Н из раствора. [40]
 |
Структура октаэдрических кластеров типа MeXg на примене иона Мо6С14 и типа М6Х12 на примере иона Nb6Cli2. [41] |
Среди галогенидов и оксидов найдены двух -, трех - и шестиядерные кластеры. По данным рентгеноструктурного анализа, МоС1г отвечает формула [ МобС СЦ. Шесть атомов молибдена находятся в центрах граней куба, образуя октаэдр Mog; восемь атомов хлора расположены в вершинах куба, каждый атом С1 связан с тремя атрмами Мо. Внешнесферные ионы С1 - выполняют роль мостиков, объединяющих кластеры [ Мо6С18 ] 4 между собой. [42]
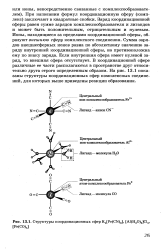 |
Структуры координационных сфер K4 [ Fe ( CN6 ], [ A1 ( H2O 6 ] C13, [ Fe ( CO5 ]. [43] |
При написании формул координационную сферу ( комплекс) заключают в квадратные скобки. Заряд координационной сферы равен сумме зарядов комплексообразователя и лигандов и может быть положительным, отрицательным и нулевым. Ионы, находящиеся за пределами координационной сферы, образуют внешнюю сферу комплексного соединения. Сумма зарядов внешнесферных ионов равна по абсолютному значению заряду внутренней координационной сферы, но противоположна ему по знаку заряда. Если внутренняя сфера имеет нулевой заряд, то внешняя сфера отсутствует. В координационной сфере различные ее части располагаются в пространстве друг относительно друга строго определенным образом. На рис. 13.1 показаны структуры координационных сфер комплексных соединений, для которых выше приведены реакции образования. [44]
Гексафториды палладия с участием Mg, Ca, Zn и Cd изо-структурны и кристаллизуются в типе гексагонального LiSbFe. Данных по аналогичным соединениям платины не имеется. Гексафториды палладия и платины с участием Sr и Ва изо-структурны и принадлежат к структурному типу гексагонального BaSiFe. Различие между типами LiSbFe и BaSiFe заключается в величине координационных чисел внешнесферных ионов. [45]
Страницы: 1 2 3 4