Многовалентный ион
Cтраница 1
Многовалентные ионы, проявляющие более высокую адсорбционную способность, коагулируют золь в меньших концентрациях, чем одновалентные ионы, так как последние в меньшей степени снижают заряд коллоидной частицы. [1]
 |
Плотность распределения смеси интактных и инактивированных клеток Е. coli M-17 по значению f - потенциала. [2] |
Многовалентные ионы могут изменять знак коллоидных частиц на противоположный. Подобное явление наблюдается у бактериальных клеток и вирусов. Добавление электролитов приводит к сжатию двойного электрического слоя ионов. [3]
Многовалентные ионы воздействуют на растрор полимера в буферной жидкости: снижают его вязкость, повышают подвижность. [4]
Многовалентные ионы имеют больший электрический заряд, чем одновалентные, но двигаются медленно в силу большой гидратной оболочки. [5]
Многовалентные ионы и Т1 катали шруют гидролиз оксалатного и малонатного эфиров, а ионы щелочных металлов имеют лишь небольшой отрицательный солевой эффект на скорость реакций эфиров адипиновой и себациновой кислот. [6]
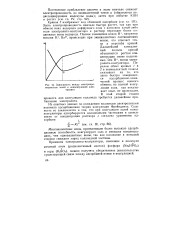 |
Зависимость между электропроводностью золей и концентрацией электролита. [7] |
Многовалентные ионы, проявляющие более высокую адсорбционную способность, коагулируют золь в меньших концентрациях, чем одновалентные ионы, так как последние в меньшей степени снижают заряд коллоидной частицы. [8]
Многовалентные ионы адсорбируются сильнее одновалентных. Ионы одинаковой валентности также адсорбируются неодинаково в связи с отличиями в размерах и степени гидратации. [9]
Многовалентные ионы в растворе должны отсутствовать. [10]
Многовалентные ионы металлов образуют, как правило, более устойчивые комплексы с ЭДТА, чем ионы с меньшей валентностью. Аналогичным образом можно замаскировать молибден, вольфрам и ванадий, окислив их до молибдат -, вольфрамат - и ванадат-ионов, если они присутствуют в растворе в виде мешающих, образующих комплексы с ЭДТА ионов более низкой валентности. [11]
Многовалентные ионы металлов адсорбируются из водных растворов на поверхности кремнезема при условии, что значения рН раствора лежат немного ниже точки, при которой гидроокись металла начинает самопроизвольно осаждаться. Количество адсорбированного вещества изменяется с концентрацией иона в растворе, но при оптимальных условиях действует общее положение, указанное выше. [12]
Некоторые многовалентные ионы ( например, А1 и Th), обладающие большим адсорбционным потенциалом, не только легко доводят - потенциал до нуля, но и могут изменить его знак. [13]
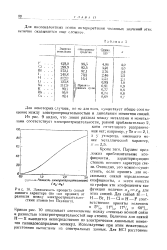 |
Зависимость процента связей. [14] |
Для многовалентных ионов интерпретация числовых значений этих величин оказывается еще сложнее. [15]
Страницы: 1 2 3 4