Многовалентный ион
Cтраница 2
 |
Зависимость подвижности ионов от температуры. [16] |
Подвижность многовалентных ионов принято относить к единице валентности, так как они несут большее количество электричества по сравнению с одновалентными ионами. [17]
Для многовалентных ионов соответствующие числа нужно еще разделить на валентность. Медь и два раствора сернокислой меди с отношением концентрации 1: 10, комбинированные в цепь, дают поэтому приблизительно вдвое меньшую электродвижущую силу, чем указанная серебряная цепь, что и было подтверждено измерениями Мозера. [18]
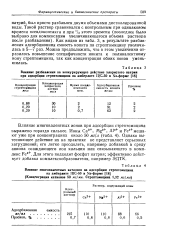 |
Влияние многовалентных катионов на адсорбцию стрептомицина. [19] |
Влияние многовалентных ионов при адсорбции стрептомицина выражено гораздо сильнее. Для этого подходит фосфат натрия; эффективно действует добавка комплексообразователя, например ЭДТК. [20]
Поглощение многовалентных ионов мембранами значительно влияет на их электрохимические свойства. Даже в том случае, если многовалентные ионы находятся в растворе в незначительном количестве, они избирательно сорбируются смолами в присутствии одновалентных ионов. [21]
Для многовалентных ионов, как, например, в случае фер-рицианид-ферроцианидной системы, величина этого слагаемого уже при ионной силе порядка 0 01 может составлять несколько десятков милливольт. [22]
Адсорбцию многовалентных ионов облегчает также разбав-ление раствора. Однако в присутствии комплексообразователей, например цитрат-ионов, тартрат-ионов, добавление кислоты усиливает сорбцию катионов металлов, так как при уменьшении рН раствора комплексные соединения разрушаются. Многовалентные катионы легче удерживаются катиоиообменными смолами, содержащими карбоксильные и другие аналогичные функциональные группы. В этом случае добавление даже небольшого количества кислоты может полностью воспрепятствовать сорбции вследствие уменьшения до нуля диссоциации карбоксильной группы как слабокислотной. [23]
У многовалентных ионов силы намного больше, и в этом случае встречаются большие отрицательные объемы. [24]
Соли, содержащие многовалентные ионы, дают промежуточные продукты гидролиза в виде основных или кислых солей. [25]
При добавлении многовалентных ионов может произойти перезарядка поверхности. [26]
В случае многовалентных ионов следует вести расчеты не на молярные, а на эквивалентные концентрации. [27]
Влияние этих многовалентных ионов на мыла достаточно известно; однако необходимо иметь в виду также их враждебность в отношении самих частиц пятнообразующего вещества. [28]
 |
Подвижности некоторых ионов при 18 С.| Изменение подвижности ионов с температурой. [29] |
В случае многовалентных ионов в выражения для чисел переноса ( 136) должны входить их скорости, деленные на валентность, так как, например, ион SO4 переносит в два раза больше электричества, чем кон С1 - при одинаковых их скоростях. [30]
Страницы: 1 2 3 4