Гель - окись - алюминий
Cтраница 2
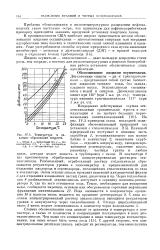 |
Температура и давление образования гидратов. [16] |
В промышленности США наиболее широко применяются методы обезвоживания жидкими осушителями - многоатомными спиртами или твердыми адсорбентами типа боксита и синтетических гелей окисей алюминия и кремния. [17]
Природные моногидратные окиси алюминия ( итальянские, французские и вообще европейские бокситы) имеют структуру бемита, но в противоположность синтетическим гелям окиси алюминия они макрокристалличны. У этих бокситов малые размеры активной поверхности ( 60 80 ж2 / й); при прокаливании они теряют воду без изменений размеров активной поверхности. [18]
Но другие исследователи считают, что вообще не существует постоянных кислотных центров на поверхности алюмосиликатного катализатора и что гель представляет собой простую механическую смесь предельно маленьких частиц силикагеля и геля окиси алюминия. Кислотность поверхности, по-видимому, должна генерироваться на твердом веществе в ответ на приближение основания, которое вызывает обратимые кристаллографические изменения в местах контакта частиц силикагеля и геля окиси алюминия. В присутствии основания некоторые ионы алюминия и кислорода, тесно примыкающие к тетраэдру окиси кремния, принимают тетраэдрическую форму с одновременным появлением кислотности; при удалении основания они снова приобретают форму некислого состояния. [19]
Адсорбирующие, дегидратирующие и каталитические свойства этих двух j типов окиси алюминия заметно различаются из-за различных размеров активной поверхности п поведения при нагревании; точно так же сильно различаются по своим свойствам природные продукты с тем же химическим составом. Гели окиси алюминия, осажденные в горячем состоянии соляной кислотой, имеют микрокристаллическую структуру и состав их приблизительно соответствует формуле 2А1203 ЗН20, слегка отклоняясь от нее в зависимости от способа и условий осаждения. [20]
Приготовление, например, двуокиси титана заключается во взаимодействии четыреххлористого титана с гидроокисью аммония с последующей промывкой, сушкой и прокаливанием образовавшегося геля. Аналогично получают гель окиси алюминия. Большинство из полученных таким образом катализаторов имеют значительную поверхность при различной степени гидратации. [21]
Адсорбенты, характеризующиеся интрамицеллярной структурой, могут иметь гомео - или гетерокапиллярную природу. Примером адсорбентов гетерокапиллярной структуры могут служить синтетические гели окиси алюминия или двуокиси кремния, а также активный уголь. [22]
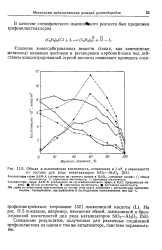 |
Общая и льюисовская кислотность, отнесенная к 1 м2, в зависимости. [23] |
Збе серии катализаторов приготовлены на основе геля окиси алюминия с механическим перемешиванием, промыванием, высушиванием и последующим прокаливанием при 550 С. [24]
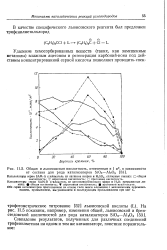 |
Общая и льюисовская кислотность, отнесенная к 1 м2, в зависимости. [25] |
Обе серии катализаторов приготовлены на основе геля окиси алюминия с механическим перемешиванием, промыванием, высушиванием и последующим прокаливанием при 550 С. [26]
КОЙ плотностью, высокой пористостью и большой удельной поверхностью сушку водной суспензии, содержащей до 32 % окиси алюминия, рекомендует проводить парами сциртог Cj-Cg до содержания окиси алюминия - 50 % мае. Румынский институт нефтехимии [128] предлагает способ обработки сухогс геля окиси алюминия в автоклаве в присутствии 0 5 - 2 % - ного водного аммиака при температуре 150 - 250 С в течение 2 - 12 ч с последующей сушкой и прокаливанием. [27]
Можно ожидать поэтому, что молекулярная структура конечных частиц имеет только ближний, а не дальний порядок. В этом отношении силика-гель и алюмосиликатный гель отличаются от геля окиси алюминия, который обычно представляет собой структуру бемита А1 ( ОН) и байерита или гиббсита А1 ( ОН) з после сушки при 120 Си структуру у - АЬОз или других безводных форм окиси алюминия после прокалки при температуре выше 540 С. Предполагают, что в гелях окиси алюминия могут находиться неизометрические первичные частицы. Элкин, Шалл и Росс [94] нашли, что алюмосиликатные гели, приготовленные гидролизом алюминиевой соли в присутствии силикагеля или даже смешением влажного силикагеля с влажным гидрогелем окиси алюминия, были аморфными для всех составов при содержании окиси алюминия до 31 % вес. [28]
При рН, равном 7, и гель двуокиси кремния и гель окиси алюминия адсорбируют небольшие количества ионов из раствора, а поэтому величины избыточного натрия были исправлены путем вычитания небольшого количества ионов натрия, адсорбировавшегося механической смесью силикагеля и алюмогеля, соответствовавшей обоим компонентам в совместно осажденном геле. [29]
Но другие исследователи считают, что вообще не существует постоянных кислотных центров на поверхности алюмосиликатного катализатора и что гель представляет собой простую механическую смесь предельно маленьких частиц силикагеля и геля окиси алюминия. Кислотность поверхности, по-видимому, должна генерироваться на твердом веществе в ответ на приближение основания, которое вызывает обратимые кристаллографические изменения в местах контакта частиц силикагеля и геля окиси алюминия. В присутствии основания некоторые ионы алюминия и кислорода, тесно примыкающие к тетраэдру окиси кремния, принимают тетраэдрическую форму с одновременным появлением кислотности; при удалении основания они снова приобретают форму некислого состояния. [30]
Страницы: 1 2 3