Гель - окись - хром
Cтраница 2
Работа Бервелла и Литтлвуда [26] по обмену - гексана с дейтерием над гелем окиси хрома важна еще и потому, что она является одной из немногочисленных работ, где для обмена насыщенных углеводородов с дейтерием применялся окисный катализатор. [16]
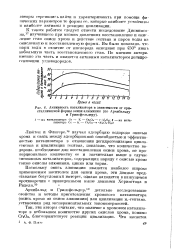 |
Активность катализатора в зависимости от кристаллической формы окиси алюминия ( по Арчибальду и Гринсфельдеру. [17] |
К таким работам следует отнести исследование Диккинсо-на 17 изучившего при низких давлениях восстановление и окисление геля окиси хрома и действие гептана и паров воды на окисленную и восстановленную формы. Им было показано, чтс пары воды в отличие от кислорода окисляют при 450 лишь небольшую часть восстановленного геля. По мнению автора, именно эта часть и является активным катализатором дегидрогенизации углеводородов. [18]
Поверхность геля окиси хрома, примененного Хоу-ардом, неизвестна, но Б руна yep и Эммет [71] приготовили гель окиси хрома таким же методом и определили его поверхность по адсорбции азота. [19]
Тейлор и Туркевич [129] получали чистые ароматические углеводороды из я-гексана при медленном движении струи гексана при 468 С над гелем окиси хрома как катализатором. [20]
В лаборатории автора было произведено магнитное изучение процесса обезвоживания геля двуокиси марганца, причем оно сходно с описанным выше для геля окиси хрома. Как и в табл. 3, указанный режим отвечает последовательному обезвоживанию. [21]
В промышленных установках процесс проводят с движущимся слоем шарикового катализатора ( 32 % Сг203 - 68 % А120, ) i полученного совместным осаждением гелей окиси хрома и окиси алюминия. Изготовитель катализатора не известен. [22]
Таким же образом Берелл и сотрудники [37] нашли, что эти представления могут быть применены и к реакциям углеводородов и дейтерия на л-комплексах на геле окиси хрома, связанных с поверхностью тем же путем, что и в соединениях типа ферроцена. Согласно Руни и сотрудникам [38], это позволяет объяснить картину обмена с дейтерием, наблюдающуюся на большом числе поли-метилциклопентанов. В частности, они предположили, что такие комплексы могут соединяться с водородом из газовой фазы или с физически адсорбированным водородом, а также и с водородом, хемосорбированным на поверхности. [23]
Гель окиси хрома может быть приготовлен осаждением гидроокиси из раствора - нитрата соли с последующим медленным обезвоживанием. Имеется несколько других методов, одним из которых является медленное восстановление из щелочного раствора хромата. При прокаливании эти гели обычно обнаруживают явление раскаливания, во время которого они превращаются в кристаллическую окись хрома. [24]
Аморфный гидрогель образуется в результате реакций поликонденсации, по типу напоминающих образование геля двуокиси кремния, и общая морфология структуры гидрогеля окиси хрома близка к морфологии гидрогеля двуокиси кремния. Непрокаленный гель окиси хрома всегда или аморфен, или в лучшем случае очень слабо упорядочен. [25]
Приготовление геля окиси хрома по Фрею и Хаппке [ 81 обеспечивает получение активного катализатора дегидрирования парафиновых углеводородов. Кристаллогидрат нитрата хрома ( 800 г) растворяют в 8 л дистиллированной воды и затем фильтруют для получения прозрачного раствора. К этому раствору добавляют 400 г ацетата аммония, растворенного в 16 л воды. [26]
Вопрос об отравляемости окиси хрома изучен еще очень мало. Водяной пар сильно адсорбируется гелем окиси хрома и вызывает временное отравление каталитической активности. [27]
Брунауер и Эммет [71] приготовили гель окиси хрома таким же методом и определили его поверхность по адсорбции азота. [28]
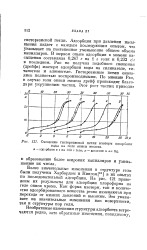 |
Смещение гистерезисной петли изотерм адсорбция. [29] |
Более значительные изменения в структуре геля были получены Харбардом и Кингом [81] в их опытах по последовательной адсорбции. На рис. 121 приведены их результаты для адсорбции хлороформа на геле окиси хрома. Как форма изотерм, так и количество адсорбированного вещества резко изменяются при переходе от низких давлений к высоким. Это указывает на значительные изменения как поверхности, так и структуры пор геля. [30]
Страницы: 1 2 3