Гель - окись - хром
Cтраница 3
 |
Смещение гистерезисной петли изотерм адсорбции. [31] |
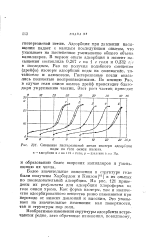
Более значительные изменения в структуре геля были получены Харбардом и Кингом [ el ] в их опытах по последовательной адсорбции. На рис. 121 приведены их результаты для адсорбции хлороформа на геле окиси хрома. Как форма изотерм, так и количество адсорбированного вещества резко изменяются при переходе от низких давлений к высоким. Это указывает на значительные изменения как поверхности, так и структуры пор геля. [32]
Как уже отмечалось выше, ЭПР весьма удобен для изучения обменного взаимодействия в магнитно-концентрированных системах с сильным обменом между парамагнитными частицами. Примеромтакого использования метода ЭПР может служить работа Ю. И. Печерской и В. Б. Казанского [27], в которой был изучен процесс термической активации геля окиси хрома при параллельном измерении активности катализаторов в реакции гидрирования этилена. Хромогель, осажденный аммиаком из водного раствора нитрата и высушенный при 100 С, содержит большое количество структурной воды и совершенно не активен в реакции гидрирования этилена. [33]
 |
Температуры соответствующие нулевым значениям свободной энергии. [34] |
Однако в присутствии соответствующих катализаторов дегидрогенизация некоторых высших парафинов может быть также основной реакцией. Фрей и Хупке [38] нашли, что пропан и бутаны дегидроге-низируются при температурах от 350 до 500 С при атмосферном давлении в присутствии геля окиси хрома. Продукты реакции состояли, главным образом, из водорода и олефина с тем же числом углеродных атомов. Нормальный бутан дает нормальные бутилены, а изобутан - изобутилен. [35]
Хорошо известно, что многие окислы переходной группы могут быть приготовлены в очень раздробленном или гелеобразном состоянии, которое дает размытые рентгенограммы. Такие неорганические гели часто получаются с целью использования их в качестве катализаторов. Например, гель окиси хрома часто применяется в реакциях гидрирования. О таких веществах, повиди-мому, более точным будет говорить, что они сами для себя являются носителями, так как они только с точки зрения классификации отличаются от катализаторов, нанесенных на инертные вещества. Некоторые характерные магнитные свойства коллоидной гидроокиси железа известны уже давно, но только недавно стало понятно, что некоторые из этих явлений обнаруживаются почти у всех гелеобразных окислов элементов переходной группы. Теория этого эффекта еще не столь хорошо развита, как в случае окислов на посторонних носителях, однако для подобных коллоидных систем, о которых рентгеновский метод дает мало или совсем не дает сведений, полезны любые новые данные о структуре. [36]
Для получения вещества с максимальной каталитиче - ской активностью необходимо проводить реакцию при нагревании до возможно более полного восстановления хромового ангидрида. При приготовлении геля окиси хрома по описанному методу можно считать, что ионы Cr 4, образовавшиеся в процессе восстановления, соединяются с неизмененной хромовой кислотой, образуя хромат трехвалентного хрома. [37]
Фрей и Гуппке показали в своей работе, что в соответствующих условиях возможно избирательное дегидрирование, причем чрезмерное увеличение температуры и времени контакта способствует реакциям крекинга. Как правило, в результате таких реакций образуется больше водорода, чем олефинов, хотя для изобутана наблюдается образование значительного количества метана, в связи с чем выход водорода снижается. Катализаторы из геля окиси хрома, примененные в ранних работах Фрея и Гуппке, оказались недолговечными. Этими же авторами [17] был запатентован более стойкий хромовый катализатор с добавкой в качестве стабилизатора окиси алюминия. После этого в литературе появились сообщения о многочисленных модификациях алюмохромовых катализаторов; окиси хрома и алюминия до настоящего времени продолжают входить в состав лучших катализаторов, применяющихся для дегидрирования бутана в бутены и бутадиен. [38]
Гель окиси хрома ведет себя как типичное парамагнитное вещество, восприимчивость которого подчиняется закону Кюри - Вейсса при среднем значении константы Вейсса. Это указывает на сравнительно небольшую степень обменного взаимодействия между соседними ионами Сг3; на основании этого можно дать модель геля Сг2Оз, согласующуюся с очень большой удельной поверхностью, которой часто обладают эти вещества. Таким образом, гель окиси хрома резко отличается от кристаллической а-окиси, в которой обменное взаимодействие соседних ионов Сг3 настолько велико, что вещество является скорее антиферромагнитным, чем парамагнитным. [39]
В качестве носителя для большей части окисных катализаторов применяется предпочтительно МОДифшмщш окиси алюминия; однако этот носитель сам не обладает каталитической активностью. Из рассмотрения способов приготовления катализаторов видно, что они должны быть в аморфном или по меньшей мере микрокристаллическом состоянии. Типичным примером могут служить катализаторы на основе геля окиси хрома. Активные катализаторы могут быть приготовлены как осаждением, так и пропиткой носителей типа активированной окиси алюминия. Окислы в виде геля или микрокристаллов обычно имеют большую удельную поверхность. Это относится и к таким носителям, как активированная окись алюминия. [40]
Из приведенного краткого образца видно, что применение метода ЭПР к проблемам, связанным с гетерогенным катализом, находится лишь в самом начале своего развития. Большинство работ посвящено изучению структуры катализаторов, в то время как с точки зрения общих представлений о механизме катализа гораздо больший интерес представляет изучение хе-мосорбции на парамагнитных активных центрах, природы образующейся при этом химической связи и промежуточных активных веществ в ходе каталитического процесса. Наиболее четко эта связь прослежена до настоящего времени в случае геля окиси хрома. Если эти наблюдения будут подтверждены на других системах и если удастся показать, что такая взаимосвязь действительно является существенной в сколько-нибудь значительном числе известных каталитических процессов, то откроются совершенно новые возможности подхода к анализу механизма каталитического действия с учетом возможных эффектов дальнодействия в многоэлектронных системах реагенты - катализатор. [41]
Удельная поверхность окиси хрома снижается с увеличением температуры термообработки. Начальная удельная поверхность дегидратированной, например при 370 К, окиси сильно зависит от условий приготовления и обычно колеблется в интервале 80 - 300 м2 / г. Данные Дерена и др. [61] и Каррозерса и др. [58] показывают, что удельная поверхность гелей, дегидратированных нагреванием на воздухе, относительно слабо зависит от температуры, если она превышает приблизительно 770 К, и составляет 10 - 30 м2 / г. Однако, если дегидратация ведется в инертном газе, заметная зависимость удельной поверхности от температуры наблюдается вплоть до примерно 970 К. Окись хрома с высокой удельной поверхностью, более 200 м2 / г, конечно, имеет микропористую структуру с порами эквивалентным диаметром менее 2 нм; после рекристаллизации до а - Сг2О3 микропоры исчезают. По данным [62], гель окиси хрома, полученный с использованием гидролиза мочевины и обезгаженный при температуре ниже 470 К, характеризуется однородными порами весьма малого диаметра и проявляет мо-лекулярно-ситовые свойства. [42]
Различные виды слоистых гелей подвергаются обработкег аналогичной обработке образцов пористого стекла. Пери и Ханнан [41] предложили метод приготовления гелей различных типов в слоистой форме, подходящей для ИК-исследования. Методика приготовления аэрогеля 7 - киси алюминия основана на получении 7 % - ного золя окиси алюминия, синтезированного из алюминия высокой степени чистоты действием уксусной кислоты в присутствии окиси ртути. Золь собирают на поверхности плотной жидкости типа ртути, чтобы получить слой желаемой толщины, затем, действуя на него аммиаком, превращают его в гель. Погружая аквагель в метиловый спирт, его превращают в алкогель, спирт удаляют нагреванием выше критической температуры. Затем аэрогель прокаливают при 600 С и получают самоподложковую вафлю из окиси алюминия, имеющую удельную поверхность около 300 м2 / г. Найдено, что пластина толщиной 2 5 мм ( оптическая толщина 40мг / см2) имеет величины пропускания, представленные ниже в таблице. Эта методика была также использована для получения силикагеля, гелей окиси хрома и смешанных окисных гелей. По-видимому, таким путем можно приготовить прекрасные образцы для ИК-исследования из ряда других окислов. [43]
Страницы: 1 2 3