Гем-группа
Cтраница 2
Он имеет относительную молекулярную массу 64 500 и содержит четыре гем-группы, связанные с четырьмя белковыми цепями. Различие между гемоглобином и миоглобином заключается в их поведении по отношению к кислороду и в подвижности четырех цепей. Если тетрамерный гемоглобин разрушается до димера или мономера, эти различия исчезают. [16]
Исходя из этого подсчитано, что длина связи Fe-N в гем-группе должна быть равной 218 пм. Ранее указывалось, что координация железом кислорода приводит к спариванию электронов. Низкоспиновый атом Fe11 на 17 пм меньше, чем высокоспиновый. [17]
Быстрое протекание реакции гемоглобина является достаточным указанием на то, что гем-группы располагаются плоско на поверхности протеиновой молекулы. Рентгенографические исследования показывают, что молекулы гемоглобина жестки и непроницаемы для жидкости, а кристаллический окси - или карбоксигемоглобин может быть превращен в метгемоглобин без всякого изменения кристаллической структуры. Кристаллы кислого метгемоглобина, взвешенные в растворе сернокислого аммония, можно без всякого изменения размеров элементарной ячейки превратить в щелочной метгемоглобин добавлением циаммоний-фосфата, а прибавлением азида натрия - в азид-метгемоглобин. Таким образом, эти реакции между геминовыми группами и ионами, диффундирующими через кристаллизационную жидкость, показывают, что геминовые группы расположены на поверхности, а постоянство размеров элементарной ячейки свидетельствует о том, что эти группы не участвуют в связи между соседними молекулами гемоглобина в кристаллической решетке. [18]
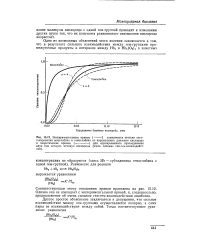 |
Экспериментальные кривые (. [19] |
Другое простое объяснение заключается в допущении, что сильное взаимодействие между гем-группами осуществляется попарно, а сами пары не взаимодействуют между собой. [20]
В работах [38, 39] предложен механизм процесса переноса кислорода, рассматривающий взаимодействие четырех гем-групп в гемоглобине. [21]
Хорошее соответствие с экспериментом получается в том случае, если предположить, что гем-группа, присоединившая кислород ( НЬОг), повышает константу связывания кислорода в 12 раз на каждую соседнюю группу и что гем-группы расположены по углам квадрата. [22]
Имидазольная группа гистидинового остатка, соединенная с атомом железа, также должна сместиться к гем-группе, что вызовет прогибание белковой цепи. Такая деформация белковой цепи способствует повышению активности другой гем-группы гемоглобина. Полностью насыщенная кислородом ( четыре молекулы СЬ) молекула гемоглобина достигает клеток тканей и высвобождает кислород. При отрыве каждой молекулы С2 молекула гемоглобина перестраивается и снижает способность отдавать оставшиеся молекулы кислорода. [23]
Перемещение атома железа и соответственно гистидинового остатка вызывает нарушение исходной конфигурации глобина и влияет на связь между собой других гем-групп. Изменение в конфигурации белковых цепей соответствует приблизительно изменению энергии на 12 - 14 кДж / моль ( сродство к кислороду) при присоединении молекулы кислорода к гемоглобину. Это фундаментальное различие в энергетике кислородного связывания объясняет зависимости, приведенные на рис. 18.9. Имеется один или несколько факторов, препятствующих смещению атома железа в порфириновое кольцо свободного гемоглобина. [24]
В случае гемоглобина предполагалось, что некоторые окислительно-восстановительные реакции могут протекать по внутримолекулярному механизму, поскольку четыре реагирующих гем-группы связаны с одной и той же молекулой. Такой механизм, в частности, был разработан Лембергом и Леггом [5] для объяснения самоокисления гемоглобина. Реакция самоокисления привлекала относительно мало внимания, но, поскольку эта реакция имеет большое значение при исследовании стабильности оксигемоглобина, она будет здесь подробно обсуждена. [25]
Молекула гемоглобина человека, подобно гемоглобину других млекопитающих, состоит из четырех полипептидных цепей ( каждая из которых содержит одну гем-группу) и способна обратимо присоединять четыре молекулы кислорода. Уже много лет назад было показано, что равновесное связывание кислорода гемоглобином описывается S-образ-ной кривой, приведенной на рис. 15.12, которая отличается от аналогичной кривой для миоглобина. [26]
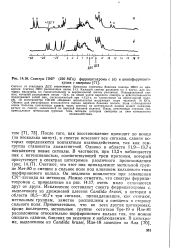 |
Спектры ПМР ( 220 МГц феррицитохрома с ( а и цианоферрицито. [27] |
После того, как восстановление проходит до конца ( за несколько минут), в спектре исчезают все сигналы, сдвиги которых определяются контактным взаимодействием, так как гем-группа становится диамагнитной. Однако в области 11 9 - 13 71 появляются новые сигналы. Считают, что этот пик принадлежит метальной группе Мет-80 и смещен в сильное поле под влиянием кольцевого тока порфиринового кольца. Он медленно появляется при замещении СК - - лиганда на метионин. Можно отметить, что спектры феррици-тохромов с, приведенные на рис. 14.17, очень мало отличаются друг от друга. Исключение составляет спектр феррицитохрома с, выделенного из дрожжевой плесени Candida krusei, в котором в области 10 5 - 10 7т три сигнала, принадлежащие, как считают, метальным группам, заметно расщеплены и смещены в сторону сильного поля. Примечательно, что во всех других цитохромах, кроме последнего, метальные группы остатков Тре-19 и Иле-81 расположены относительно порфиринового кольца так, что можно ожидать сдвигов, близких по величине к наблюдаемым. [28]
Мы детально рассмотрим влияние рН ( или pD), температуры, растворителя, состояния окисления и связывание малых молекул на спектры отдельных белков, в том числе содержащих гем-группы и другие простетические группы, резонансные сигналы и влияние которых мы еще не рассматривали. Эффект кольцевых токов ( см. разд. Мы обсудим также большое число других факторов, влияющих на химические сдвиги, и другие методы наблюдения, которые лучше всего рассматривать в их конкретных приложениях. Большая часть наблюдаемых спектров получена с использованием накопления большого числа прохождений ( иногда 100 и более) с помощью накопителя ( см. разд. [29]
Хорошее соответствие с экспериментом получается в том случае, если предположить, что гем-группа, присоединившая кислород ( НЬОг), повышает константу связывания кислорода в 12 раз на каждую соседнюю группу и что гем-группы расположены по углам квадрата. [30]
Страницы: 1 2 3 4