Гем-группа
Cтраница 4
 |
Аллостерическое гем-гем-взаимодействие в димере. [46] |
Примером могут служить цито-хромы, присутствующие в каждом живом организме. Они содержат гем-группы, связанные с белком иначе, чем в молекулах миоглобина и гемоглобина. Интересным является белок, содержащий негемовое железо ( так называемый высокопотенциальный железосодержащий белок), выделенный из клеток нескольких видов пурпурных бактерий. Он может обратимо одноступенчато ( путем потери одного электрона) окисляться ионом гексацианоферрат ( Ш) кислоты [ Fe ( CN) e ] 3 - и другими окислителями и, вероятно, катализирует какие-то окислительные процессы, важные для физиологии бактерий. [47]
Эти гем-белки обнаруживаются как в животных, так и в растительных клетках и играют роль переносчиков электронов. Они принимают электрон от вещества, являющегося немного более сильным восстанавливающим агентом, и передают его более сильному окислителю. В цитохромах атом железа гем-группы также координирован на атоме азота имидазольного кольца с одной стороны от плоскости порфиринового цикла. Но в дополнение к этому он координирует с другой стороны атом серы метионинового остатка, который может находиться в разных частях белковой цепи. Поэтому потенциальная способность атома железа в цитохроме ( к связыванию кислорода подавлена. [48]
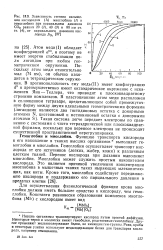 |
Зависимость степени насыщения кислородом ( А миоглобина ( Л и гемоглобина при парциальном давлении СО2, равном 20 ( 2, 40 ( 3 и 80 мм рт. ст. ( 4, от парциального давления кислорода Ро2 1271. [49] |
Низшие организмы транспортируют кислород путем простой диффузии. Некоторые черви и моллюски имеют гемобелки, родственные гемоглобину. Другие применяют железосодержащие белки, не имеющие гем-группы. Раки, крабы и некоторые улитки используют медьсодержащие белки для транспорта кислорода, например гемоцианин. [50]
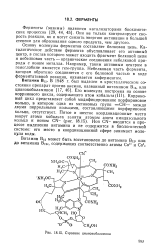 |
Строение цианокобаламина. [51] |
Основу молекулы ферментов составляет белковая цепь. Каталитическое действие фермента обусловливает его активный центр, в состав которого может входить фрагмент белковой цепи и небелковая часть - органические соединения небелковой природы с ионом металла. Например, таким активным центром в гемоглобине является гем-группа. Небелковая часть фермента, которая обратимо соединяется с его белковой частью в ходе ферментативной реакции, называется коферментом. [52]
 |
Стереоскопическое изображение пространственной конфигурации молекулы гемоглобина кольчатого червя Glycera. [53] |
Каждая пептидная группа CCONHC обозначена прямым отрезком, соединяющим два кружка, которые соответствуют положению в пространстве а-атомов углерода, принадлежащих 150 или 146 аминокислотным остаткам. На рисунке ясно видно несколько участков - спирали. Атом железа, показанный более крупным кружком в центре почти плоской гем-группы, образует шесть связей: четыре с атомами азота гем-группы, одну с атомом азота имидазольного кольца боковой цепи гистидина ( остаток № 90, считая от свободного МН2 - конца полипептидной цепи) и одну с атомом кислорода, принадлежащего молекуле связываемого гемоглобином кислорода ( кружок слева от плоскости тема), или с атомом углерода молекулы окиси углерода. [54]
Вторичные структуры миоглобина и гемоглобина представлены главным образом а-спиралями. Восемь отрезков полипептидной цепи являются относительно прямолинейными а-спиралями; эти отрезки содержат 80 % аминокислотных остатков всей цепи, остальные 20 % остатков приходятся на места сгибов, соединяющие между собой - спиральные отрезки. При укладывании цепи ( третичная структура) образуется полость, в которой расположена гем-группа. [55]
Миоглобин связывает кислород и сохраняет, его в мышце до тех пор, пока он не потребуется для метаболического окисления. Каждая молекула миоглобина представляет собой одну цепь из 153 аминокислотных остатков ( молекулярная масса 17800), связанную с одной гем-группой. [56]
Каждая пептидная группа CCONHC обозначена прямым отрезком, соединяющим два кружка, которые соответствуют положению в пространстве а-атомов углерода, принадлежащих 150 или 146 аминокислотным остаткам. На рисунке ясно видно несколько участков - спирали. Атом железа, показанный более крупным кружком в центре почти плоской гем-группы, образует шесть связей: четыре с атомами азота гем-группы, одну с атомом азота имидазольного кольца боковой цепи гистидина ( остаток № 90, считая от свободного МН2 - конца полипептидной цепи) и одну с атомом кислорода, принадлежащего молекуле связываемого гемоглобином кислорода ( кружок слева от плоскости тема), или с атомом углерода молекулы окиси углерода. [57]
С другой стороны, Кейлин и Хартри [16, 17] нашли, что в присутствии азид-ионов восстановление происходит, если добавляется перекись водорода. Природа этой реакции неизвестна. Она могла бы быть результатом наличия в молекуле каталазы четырех гематино-вых групп и того, что азид, соединяясь с одной группой, изменяет окислительно-восстановительные свойства остальных групп подобно тому, как это имеет место при взаимодействии гем-групп в реакции гемоглобина с кислородом, но это маловероятно, потому что азид-каталаза, как и свободная каталаза, устойчива по отношению к другим восстановителям и даже к гидросульфиту натрия. [58]
Процесс транспортировки кислорода от легких к мышцам осуществляется следующим образом. Парциальное давление кислорода в легких высоко, поэтому кислород координируется гемоглобином. Затем он транспортируется кровью к ткани, где давление кислорода низкое; в этом случае кислород отщепляется от гемоглобина и присоединяется к миоглобину. В молекуле миоглобина полипептидная цепь координирована железом гем-группы так же, как в гемоглобине. Однако в отличие от гемоглобина, где на одну молекулу приходится четыре гем-группы, одна молекула миоглобина содержит одну гемовую единицу. [59]
Известна последовательность аминокислот [47] и конформация цепи [48-51] миоглобина кашалота. Это был первый белок, структура которого определена с помощью рентгеноструктурного анализа. Молекулу можно рассматривать как корзину, состоящую из восьми спиралей, которая содержит гем-группу внутри гидрофобной полости. [60]
Страницы: 1 2 3 4