Гемоглобин - человек
Cтраница 1
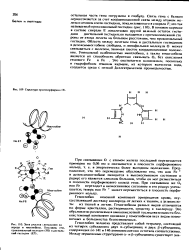 |
Структура протопорфирина IX.| Зона участка связывания кл лоро да в миоглоби не. Пока за ны гем, проксимальный гистидин ( F8 и днстальный гистидин ( Е7. [1] |
Гемоглобин человека представляет собой тетрамер, состоящий из четырех субъединнц: двух а-субъеднннц и двух р - субъединиц, содержащих по 141 и 146 аминокислотных остатков соответственно. [2]
Гемоглобин человека содержит 0 335 % железа. [4]
Гемоглобин человека имеет несколько разновидностей. В течение первого года жизни фетальный гемоглобин почти полностью заменяется гемоглобином взрослых. Весьма существенно, что фетальный НЬ обладает более высоким сродством к Ог, чем гемоглобин взрослых, что позволяет ему насыщаться при более низком напряжении кислорода. Гем разных гемоглобинов одинаков, глобины же отличаются по своему аминокислотному составу и свойствам. [5]
Молекула гемоглобина человека, подобно гемоглобину других млекопитающих, состоит из четырех полипептидных цепей ( каждая из которых содержит одну гем-группу) и способна обратимо присоединять четыре молекулы кислорода. Уже много лет назад было показано, что равновесное связывание кислорода гемоглобином описывается S-образ-ной кривой, приведенной на рис. 15.12, которая отличается от аналогичной кривой для миоглобина. [6]
Электрофокусирование гемоглобина человека в градиенте плотности на колонке Вестерберга и Свенссона ( время опы. [7]
Видовая специфичность гемоглобина человека и различных животных обусловлена не гемом ( гем имеет одинаковое строение во всех гемогло-бинах), а белковой частью - глобином. [8]
Белковая часть гемоглобина человека, глобин, состоит из четырех полипептидных цепей, попарно идентичных [48]; это две а - и две р-цепи. [9]
Известен целый ряд мутантных гемоглобинов человека, отличающихся от нормального заменой одного остатка в а - или р-цепи белка ( стр. [10]
Известен целый ряд мутантных гемоглобинов человека, отличающихся от нормального заменой одного остатка в а - или ( 3-цепи белка ( стр. [11]
Определены первичные структуры многочисленных анормальных гемоглобинов человека; некоторые из них изучены методом рентгеноструктурного анализа, что сделало возможным объяснение патологических следствий генетических ошибок на молекулярном уровне. Серповидная анемия, названная так вследствие того, что эритроциты пациентов при низких значениях р ( О2) сплющиваются, приобретая форму серпа, является причиной смерти примерно 80000 детей ежегодно. Деоксигенированная форма HbS, по-видимому, агрегирует с образованием нерастворимого полимера. Один из предложенных методов лечения анемии заключается во введении низких концентраций цианат-иона, что, как полагают, вызывает карбомоилирование аминогруппы Af-концевых остатков валина-1 в а - и р-цепях. Первый из этих остатков участвует в межцепочечном взаимодействии в дезоксигемоглобине, а второй образует электростатическую связь с 2 3-дифосфоглицератом. Кар-бамоилирование предотвращает оба типа взаимодействий, способствуя тем самым сдвигу в сторону конформации оксигемоглобина и уменьшению риска агрегирования. [12]
 |
Пептидные карты гемоглобинов человека. Денатурированный гемоглобин. [13] |
Многие изменения в структуре гемоглобина человека обусловлены. [14]
Закономерности обмена между цепями гемоглобина человека и гемоглобина собаки, происходящего в кислой среде, также согласуются со схемой асимметричной диссоциации. [15]
Страницы: 1 2 3 4