Гемоглобин - человек
Cтраница 2
Разрабатываются иа основе фторугле-родов и гемоглобина человека и животных, заключенного в искусств, газопроницаемую оболочку. [16]
Контрастирующие примеры рибонуклеазы [689], гемоглобина человека ( который присоединяет 2 3-дифосфоглицерат, АТР или инозитгексафосфат в положении между двумя р-цепями [672]) и стафилоккоковой нуклеа-зы [242] показывают, что в белках не существует единственного и универсального фосфорилсвязывающего центра. [17]
Гемоглобины животных значительно отличаются от гемоглобина человека по аминокислотному составу. Однако все они успешно выполняют функцию транспорта кислорода. Несмотря на различия в аминокислотном составе вторичная и третичная структуры гемоглобинов из различных источников подобны. N-Концевые аминокислоты у ряда гемоглобинов также одинаковы. [18]
Ингбар и Касс [116] амперометрически титровали гемоглобин человека действием AgNO3 в аммиачной среде, содержащей 0 85 % NaCl. [19]
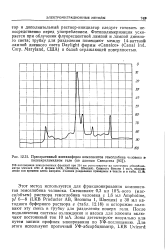 |
Препаративный изотахофорез компонентов гемоглобина человека в полиакриламидном геле ( по данным Свендсена. [20] |
Этот метод используется для фракционирования компонентов гемоглобина человека. Смешивают 0 3 мл 10 % - ного ( масса / объем) раствора гемоглобина человека с 1 6 мл Ampholine. LKB Producter AB, Bromma 1, Швеция) и 30 мл катодного буферного раствора е ( табл. 12.18) и осторожно заливают эту смесь в трубку для разделения поверх геля. Зоны детектируют визуально ила путем записи профиля элюирования по УФ-поглощению. [21]
Было показано, что коэффициент экстинкции дезоксигени-рованного гемоглобина человека в водном растворе при рН 7 и длине волны 430 им равен 532 см2 / ммоль [61]; при этом принимали, что его мол. Чему была равна концентрация дезоксигепиро-ванного гемоглобина в растворе. [22]
При работе с гемоглобином лошади и различными гемоглобинами человека было показано, что в почти нейтральных растворах эти белки могут образовывать две различные четвертичные формы. Формы Т и R отличаются друг от друга способом упаковки полипептидных субъединиц в тетрамер. [23]
Было также обнаружено [67], что разновидность гемоглобина человека, известная как гемоглобин J Capetown, в котором одна аминокислота снцапи, аргинин-ю 92 ( iFG4), замещена на глутамин, дает тот же спектр, что и нормальный гемоглобин А человека. Этот гемоглобин, как известно, имеет большее сродство к кислороду, чем гемоглобин А. Очевидно, что это отличие не связано с изменениями в электронной структуре гемов. [24]
Данные для НЬ и его производных [3] относятся к гемоглобину человека, для миоглобина и его производных [4] - к Mb кашалота. [25]
Хотя степень участия этих водородно-связанных ионных пар в механизме оксигенации гемоглобина человека окончательно не выявлена, в работе [116] получены важные данные о роли, которую играют солевые мостики, а именно ионная пара His ( 146) / 3 - Im - ООС Аср ( 94) / 3 и комплекс, образуемый неорганическим анионом, который располагается между боковыми группами Val ( l) a и Arg ( 141) a. Таким образом, взаимодействия типа ионных пар, которые сохраняются при эволюции белкового семейства, очевидно, должны играть важную роль в поддержании структурной или функциональной целостности белков, а возможно, и того и другого. Существует множество таких взаимодействий типа ионных пар, конкретную роль которых еще предстоит установить. [26]
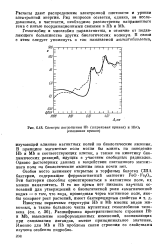 |
Спектры поглощения НЬ ( штриховая кривая и НЬО8 ( сплошная кривая. [27] |
Известны первичные структуры НЬ и Mb многих видов животных, а также большого числа мутантных гемоглобинов человека ( см. с. Расшифровка пространственного строения НЬ и Mb, выявление конформационных изменений, возникающих при связывании лигандов, имеют принципиальное значение. Именно для Mb и НЬ проблема связи строения со свойствами изучена особенно подробно. [28]
Изучение механизма взаимодействия между гаптоглобином человека, ковалентно связанным с сефарозой 4В, и гемоглобином человека, а также а - и р-цепями, обработанными я-хлормеркурибен-зоатом, проводилось двумя способами: изучалось связывание с помощью хроматографии на колонке и связывание а-цепей в равновесных условиях. Цепи - это цепи, меченные 14С с помощью п-хлормеркури - 14С ] бензойной кислоты. Связывание гемоглобина и а - и р - цепей на иммобилизованном гаптоглобине ( 38 нмоль гаптоглобина на 1 мл сефарозы 4В) показано на рис. 11.3. Добавление возрастающих количеств гемоглобина приводит к плато насыщения при 1 5 моль гемоглобина на 1 моль гаптоглобина. [29]
Другими словами, его сродство к кислороду сравнимо и даже может превышать сродство к кислороду гемоглобина человека. Другими словами, белок весьма грубыми воздействиями производит основные изменения в состоянии равновесия между комплексами Fe ( II) - nop - фиринов с координационными числами 4 5 и 6, но лишь слегка уточняет состояние равновесия, включающего координирование кислорода. [30]
Страницы: 1 2 3 4