Нормальный гемоглобин
Cтраница 1
 |
Структура Р - ке-ратина.| Сложная спираль белка, состоящая из семи спиралей.| Модель строения миоглобина. [1] |
Нормальный гемоглобин ( А) состоит из 4 полипептидных цепочек, из которых 2, получившие название альфа, имеют по 141 аминокислотному остатку и 2 цепочки - бета содержат по 147 амино кислот. [2]
Нормальный гемоглобин F состоит из двух цепей а и двух цепей у - Первые тождественны цепям а гемоглобина А, в то время как при гидролизе цепей у образуются пептиды, отличающиеся от пептидов, полученных из цепей Р и обладающие гликокольным остатком у аминного конца. [3]
Во всех нормальных гемоглобинах и миоглобинах млекопитающих имеется дистальный гистидин, и первоначально предполагалось, что он играет существенную роль в обратимом связывании кислорода путем, например, образования водородной связи. [4]
СН ( СН3) 2 у нормального гемоглобина, тогда как серповидный гемоглобин имеет в этом месте отрицательно заряженную боковую цепь - СН-СН2СОСГ. Молекула гемоглобина является димером с двумя симметричными половинами, так что разность зарядов определяется этими двумя частями. [6]
Гемоглобин S таких серповидных клеток отличается от нормального гемоглобина лишь одним аминокислотным остатком в fJ - цепях, В нем происходит замена полярной глутаминовой кислоты на неполярную аминокислоту валин, что приводит к очень сильному снижению растворимости дезоксигемоглобина S, хотя растворимость оксигемоглобина при этом остается нормальной. Дезоксигемоглобин S образует волокнистый осадок, который вызывает деформацию и разрушение эритроцитов и как следствие - хроническую гемолитическую анемию. [7]
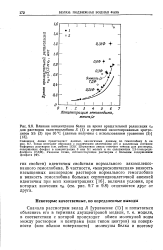
В частности, макроскопическая вязкость насыщенных кислородом растворов нормального гемоглобина и вязкость гемоглобина больных серповидноклеточной анемией идентичны при всех концентрациях [16], включая условия, при которых значения тд ( см. рис. 9.7 и 9.8) отличаются друг от друга. [9]
 |
Взаимное расположение иона имидазолия остатка ги стадии а и атома железа в гемоглобине. Положительный заряд имида-золия сохраняет ион Fez. [10] |
Прежде всего необходимо объяснить, почему соединения железа ( II) устойчивы в нормальном гемоглобине. [11]
Данные, приведенные на рис. 9.7 и 9.8, были одними из первых [12], которые указали на различие в поведении нормального гемоглобина взрослого человека и гемоглобина больных серповидноклеточной анемией. [12]
У людей, страдающих серповидной анемией, синтезируется гемоглобин, в котором всего лишь одна аминокислота из нескольких сотен отличается от соответствующей аминокислоты в нормальном гемоглобине. Однако продолжительность человеческой жизни от этого заметно уменьшается. [13]
В 1949 г. Полинг, Итано, Сэнгер и Уэллс обнаружили, что гемоглобин больных серповидноклеточной анемией, HbS, отличается по своей электрофоретической подвижности от нормального гемоглобина человека, НЬА. Это исследование, в котором было обнаружено различие зарядов двух форм молекул гемоглобина, положило начало изучению молекулярных болезней крови. Генетики установили, что серповидноклеточная анемия наследуется по простым менделевским законам. Индивидуумы, гомозиготные по гену HbS, обычно умирают в раннем возрасте. В их крови часто сохраняется значительное количество гемоглобина плода, У индивидуумов, гетерозиготных по этому гену, содержится примерно 40 % HbS. [14]
 |
Некоторые мутантные гемогло-бины человека1. [15] |
Страницы: 1 2 3