Нормальный гемоглобин
Cтраница 3
Было обнаружено, что в положении 58 а-цепи гемоглобина и в положении 63 р-цепи находится остаток аминокислоты гистидина, причем его имидазольное кольцо жестко закреплено вблизи от атома железа гем-группы. Этим электростатическим эффектом иона имидазолия и объясняется необычная устойчивость атома железа ( II) в нормальном гемоглобине. [31]
Перутц и др. [32] показали, что гемоглобин S из красных кровяных телец больных так называемой серповидно-клеточной анемией является жидкокристаллическим. Эти молекулы отличаются от нормального гемоглобина А замещением лишь одной аминокислоты в последовательности 3-цепи белка. При деоксигенации этого небольшого отличия оказывается достаточным, чтобы осуществилась самоорганизация молекул гемоглобина в микроскопические трубочки, тогда как молекулы нормального гемоглобина имеют глобулярное строение. С помощью электронного микроскопа обнаружены ряды параллельных дуг [33], которые, как мы покажем ниже, соответствуют холестерической организации. [32]
Более точно - одна молекула гемоглобина представляет собой агрегат из четырех сцепленных межмолекулярными силами полиаминокислотных цепей - двух идентичных ос-цепей и двух идентичных р-цепей. Так часто бывает, что функциональный белок получается слипанием нескольких цепей. Так вот, мутация, о которой идет речь, приводит к тому, что шестой аминокислотой в р-цепи становится не Глу, как в нормальном гемоглобине, а Вал. [33]
Определенную роль в патогенезе малярии играют генетически обусловленные аномалии крови. Относительной устойчивостью к тропической малярии обладают лица, имеющие патологический гемоглобин S. У данной категории больных тропической малярией отмечается более легкое течение заболевания и отсутствие летальных исходов вследствие значительно меньшей численности паразитов в крови сравнительно с больными с нормальным гемоглобином А. [34]
Мутации в организмах могут часто приводить к изменениям в строении определенных белков, не влияющим на активный центр молекулы. При этом многие важные свойства мутантных гемоглобинов могут сильно изменяться по сравнению с нормальным ( например, растворимость, электрохимические свойства), но константа связывания молекулярногб кислорода гемоглобином при этом остается точно такой же, как у нормального гемоглобина. У изученных бактериальных ферментов известно множество мутантных форм, отличающихся, как правило, заменой одного аминокислотного звена в цепи. Многие из белков-мутантов не отличаются по ферментативной активности от белка дикого типа. С другой стороны, наблюдаются и такие мутанты, которые вовсе лишены активности, и такие, у которых каталитические свойства существенно изменены. [35]
Методом, разработанным Сенгером ( разд. У большинства млекопитающих гемоглобины имеют цепи двух типов ( называемые а - и ( 3-цепями), по две цепи каждого типа в молекуле. Последовательность аминокислотных остатков полностью известна для полипептидных цепей нормального гемоглобина человека, для многих аномальных гемо-глобинов человека ( см. разд. [36]
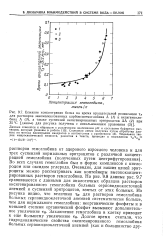
Очевидно, для наших целей эритроциты можно рассматривать как контейнеры высококонцентрированных растворов гемоглобина. На рис. 9.8 данные рис. 9.7 сравниваются с данными для аналогичных образцов растворов оксигенированного гемоглобина больных серповидноклеточной анемией и суспензий эритроцитов, взятых от этих больных. Из рисунка видно, что величина тд для растворов гемоглобина больных серповидноклеточной анемией систематически больше, чем для нормального гемоглобина: неорганические фосфаты и в меньшей степени органический фосфат вызывают дополнительное увеличение TR. Заключение гемоглобина в клетку приводит к еще большему увеличению тд. [38]
Интересно упомянуть о ситуации, когда самосборка белковых единиц в подобную структуру оказывается опасной для жизни. Таким случаем является известная наследственная болезнь - серповидно клеточная анемия, встречающаяся примерно в одном случае на 10000 человек. Гемоглобин в здоровой клетке существует в виде тетрамеров, состоящих из двух идентичных а-цепей и двух идентичных 0-цецей. У больных серповиднокле-точной анемией гемоглобин ( называемый гемоглобином S в отличие от обычного гемоглобина А) отличается от нормального гемоглобина единственным аминокислотным остатком: а-цепи этих двух гемоглобинов одинаковы, а в ( 3-цепи в гемоглобине S нормальный шестой ( начиная с JV-конца) аминокислотный остаток - глютаминовая кислота - замещен валином. В отличие от глютаминовой кислоты, в которой имеется кислая R - группа Я - группа валика является нейтральной. В настоящее время считается, что валин 06Val, находящийся на периферии тетрамера гемоглобина, являясь гидрофобным, склеивается с гидрофобным фенилаланином 085Рпе или гидрофобным лейцином 088 Leu цепи соседнего тетрамера гемоглобина, также находящимися на периферии тетрамера. [39]
С помощью электрофореза - метода, который позволяет разделять белки по их суммарному заряду - было установлено, что при рН 6 9 суммарный заряд HbS является положительным, тогда как для НЬА он отрицателен. Таким образом, впервые было показано, что болезнь вызывается дефектной молекулой гемоглобина. В 1956 г. Ингрэм показал, что различие между нормальным и аномальным гемоглобином определяется одной аминокислотой, а затем были установлены полные аминокислотные последовательности НЬА и HbS. Гемоглобин состоит из четырех полипептидных цепей ( рис. 3.36): двух а-цепей и двух ( 3-цепей длиной соответственно 141 и 146 аминокислотных остатков. Нарушение происходит в шестой аминокислоте р-цепи. В нормальном гемоглобине на этом месте должна быть глутаминовая кислота. Однако в HbS она заменена на валин. [40]
Если один из сравниваемых белков обладает какими-то отличиями в аминокислотной последовательности определенного участка первичной цепи, то пептидные фрагменты этого участка будут передвигаться по электрохроматографическому полю с иными скоростями ( а часто и в ином направлении) по сравнению с фрагментами такого же участка другого белка. В результате первые пептиды займут особое положение на пептидных картах, тогда как фрагменты из идентичных участков полипептидных цепей займут аналогичные места. Отличия в последовательности, таким образом, будут обнаружены в пятнах, имеющихся на одной электрохроматограмме и не появляющихся на другой. Элюция и количественный аминокислотный анализ лишних пептидных пятен позволяет далее установить наличие специфических для данного белка аминокислот, характеризующих эти фрагменты. Гемоглобин S отличается от нормального гемоглобина А по злектрофоретической подвижности и частично замещает последний у больных серповидно-клеточной анемией. [41]
III указывалось, что первичная структура некоторых полипептидных гормонов ( в частности, вазопрессина и меланоцитстимулирующего гормона) у разных биологических видов не вполне одинакова. Такая же видовая специфичность наблюдается и у белков. В препаратах цитохрома с, выделенных от разных видов, также были обнаружены индивидуальные различия, определяющиеся природой аминокислот в ключевом пептидном сегменте. Помимо этих вариаций, обусловленных видовой специфичностью, встречаются также и различия в белках одного и того же вида, возникшие в результате мутаций. Большинство сведений о влиянии мутаций на структуру белка почерпнуто нами из прекрасных работ Ингрэма. Ингрэм и его сотрудники показали, что нормальный гемоглобин взрослого человека и гемоглобин больных таким наследственным заболеванием, как серповидноклеточная анемия, отличаются только тем, что в определенном положении р-цепи остаток глутаминовой кислоты в аномальном гемоглобине заменен валином. Напомним, что молекула гемоглобина состоит из двух пар идентичных цепей: а - и р-цепей в гемоглобине взрослого человека или ос - и у-цепей в гемоглобине плода. [42]
Местное население нередко страдает одновременно несколькими заболеваниями. С указанными обстоятельствами связаны характерные для тропиков особенности клинического течения болезней. Некоторые заболевания в тропиках протекают более тяжело, чем в странах с умеренным климатом, например аме-биаз, туберкулез, менингококковая инфекция, брюшной тиф, дизентерия. Для других инфекций и инвазий характерно более легкое течение, нередко субклиническое. Например, у местных жителей стран Африки неоднократно наблюдались амбулаторные случаи желтой лихорадки. Причины, обусловливающие особенности течения болезней в тропиках, нередко сложны. Только в последние 10 лет удалось установить, что лица - носители атипичного гемоглобина S, болеют тропической малярией легче и значительно реже умирают от церебральной ее формы, чем лица с нормальным гемоглобином. Загадка отсутствия случаев дифтерии зева у местных жителей жарких стран раскрыта. Установлено, что у жителей Того и Нигерии имеется напряженный иммунитет к дифтерии во всех возрастных группах, кроме новорожденных. Местное население жарких стран интенсивно заражается дифтерией, но не через дыхательные пути, а через кожу. [43]
Страницы: 1 2 3