Гемопротеин
Cтраница 1
Гемопротеины относятся к сложным белкам, в состав простетической группы которых входят ион металла и порфириновое ядро. [1]
Гемопротеины широко распространены в клеточных системах и катализируют многие реакции, главным образом окислительно-восстановительные процессы, существенные для дыхания и производства энергии в ходе обмена веществ. [2]
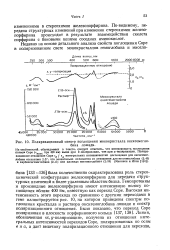 |
Поляризационный спектр поглощения монокристалла оксигемоглобина лошади. [3] |
Гемопротеины и производные железопорфирина имеют интенсивную полосу поглощения вблизи 400 нм, известную как переход Соре. Высокая интенсивность этого перехода по сравнению с другими переходами в теме иллюстрируется рис. 10, на котором приведены спектры поглощения кристалла и раствора оксигемоглобина лошади и спектр поляризационного отношения. [4]
Гемопротеины представляют собой ферменты, активным центром ( простетической группой) которых является порфири-новый комплекс железа. [5]
Другим важным гемопротеином, изученным методом мессбауэровской спектроскопии, является пероксидаза - фермент, катализирующий окисление фенолов и других подобных субстратов перекисью водорода. Маеда и др. [39-41] детально исследовали мессбауэровские спектры пероксидазы, выделенной из японского редиса, а также ее соединений с фтором, гидроксильной группой, азидом и цианидом. Для обогащения препарата изотопом 67Fe предварительно приготовляли апопероксидазу - белок, лишенный простетической группы, содержащей железо тема. Отдельно из диметилового эфира протопорфирина и обогащенного до 68 % 57Fe синтезировали протогеминхлорид, который затем хромато-графически очищали на колонке с целитом-545. Препарат тщательно очищали хроматографически от избытка протогеминхлорида и побочных продуктов реакции. [6]
В гемопротеинах ион металла находится в центре порфири-новой молекулы. Получается гемин, имеющий форму диска. [7]
 |
Модель молекулы метгемоглобина лошади, полученная на основании. [8] |
Простетическая группа гемопротеинов - железопротопорфи-рин IX - может рассматриваться как тетракоординационныи комплекс конфигурации, близкой к квадратно-плоской, с двумя ли-гандами, связанными с железом по нормали к плоскости порфи-рина. [9]
Цитохромы - это гемопротеины - белки, содержащие в качестве прочно связанной простетической группы гем. Атом железа в теме может менять валентность, присоединяя или отдавая электроны. [10]
 |
Модель структуры оксигемоглобина лошади ( разрешение 0 55 им. [11] |
Высокая способность этого гемопротеина связывать кислород позволяет личинкам комара находиться в водной среде, бедной кислородом. [12]
Хотя функции этих гемопротеинов сильно различаются несмотря на наличие общей простетической группы - железопрото-порфирина IX, мы не сможем здесь достаточно подробно обсудить взаимосвязь между структурой молекул, электронной структурой тема и функциональными особенностями всех этих белков. Подробно эти вопросы будут рассмотрены на примере гемоглобина и миоглобина, поскольку для установления взаимосвязи между стереохимией, электронными свойствами и функциональными особенностями этих двух белков можно привлечь не только информацию о структуре, полученную, при высоком разрешении, но и спектроскопические данные об электронной структуре железопорфири-новой группы. На этой основе будет подробно рассмотрено взаимодействие простетической группы с белковым окружением. [13]
Различие между четырьмя гемопротеинами - гемоглобином, мио-глобином, пероксидазой и каталазой-обусловлено только разной природой протеина, к которому присоединяется протопорфирин железа. Анализ показывает, что гемоглобин и каталаза имеют по четыре гем - или гематиновые группы в молекуле, в то время как миоглобин и пероксидаза имеют только по одной. Эти четыре гемопротеина отличаются не только молекулярным весом, но также соотношением входящих в их состав аминокислот. [14]
Все цитохромы представляют собой гемопротеины. [15]
Страницы: 1 2 3 4