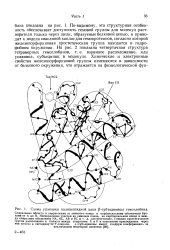
Гемопротеин
Cтраница 4
Ввиду отсутствия прямых доказательств все имеющиеся в настоящее время аргументы относительно природы этих перекисных комплексов могут основываться только на аналогиях с другими производными гемопротеинов и их реакциями. Предположение Чанса о том, что первичные комплексы каталазы испытывают атаку на порфириновое кольцо, не кажется вполне правдоподобным, если произвести сравнение с пероксидазой. Первичный комплекс пероксидазы напоминает первичный комплекс каталазы, особенно в области Соре, однако структура с видоизмененным порфириновым кольцом приписывается комплексу IV, который образуется с пероксидазой в присутствии избытка гидроперекиси алкила. В видимой области спектры первичных комплексов похожи на спектры свободных энзимов; очень большая скорость образования комплексов, а в случае каталазы преимущественное образование их в присутствии цианида - все это наводи на мысль о том, что этот процесс образования включает простое бимолекулярное замещение. Большое сродство гематиновои группы этих энзимов к перекиси водорода свидетельствует о том, что связывание молекулы Н2О2 как таковой исключается, так как этот тип реакции относится к реакциям замещения связанного аниона ОН сольватационной Н2О2, а в отношении этой реакции можно сделать вывод при учете изменений теплоты и энтропии, что она не может быть осуществлена. Интересно отметить, что соединения этого типа не ограничиваются гемо - - протеинами. [46]
Координация уменьшает ионизационный потенциал соединений закисного железа з водном растворе, вследствие чего любая эндотермическая реакция свободных ионов закисного железа становится в случае гемопротеинов менее эндотермичной и поэтому, возможно, более быстрой. [47]
Таким образом, электронные и стерео-химические ограничения, накладываемые на связывание лиганда по шестому координационному месту, приобретают первостепенное значение при описании химического и физиологического поведения гемопротеинов. [49]
Белки, в которых реакционная способность металла, входящего в состав простетической группы, определяется в основном взаимодействием белковой цепи с органическим каркасом простетической группы, например гемопротеины. [50]
По-видимому, эта структурная особенность обеспечивает доступность гемовой группы для молекул растворителя только через щели, образуемые белковой цепью, и приводит к модели масляной капли для гемопротеинов, согласно которой железопорфириновая простетическая группа находится в гидрофобном окружении. [52]
При отсутствии прямых доказательств изменения валентности или участия в реакции промежуточных соединений типа свободных радикалов полезно дать обзор данных о реакциях ионизированного железа в подобных системах, а затем проанализировать возможность осуществления подобных механизмов в реакциях гемопротеинов. [53]
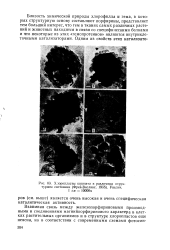 |
Хлоропласты шпината в различном структурном состоянии ( Фрей-Вислинг, 1955. Увелич. 1 см lOOOOx. [54] |
Близость химической природы хлорофилла и тема, в которых структурную основу составляют порфирины, представляет тем больший интерес, что гем в тканях самых различных растений и животных находится в связи со специфическими белками и что некоторые из этих гемопротеинов являются внутриклеточными катализаторами. [55]
Данные, свидетельствующие в пользу свободнорадикального механизма реакций между ионами закисного и окисного железа и перекисью водорода, с исчерпывающей ясностью обсуждены в статье Бак-сендаля в этом томе, и здесь необходимо лишь подытожить и обсудить те его особенности, которые имеют специальное отношение к реакциям гемопротеинов. Доказательство наличия этого механизма является по существу косвенным. Опыт показывает, что присутствуют весьма активные промежуточные соединения, и в результате обширных кинетических исследований обнаружено протекание конкурирующих реакций с образованием этих промежуточных соединений. Свободноради-кальный механизм был принят потому, что он объясняет химическую активность этой системы в окислении субстратов ( реакция Фентона) и в инициировании полимеризации винилышх соединений [84], а также дает возможность составить ряд реакций, которые в значительной степени объясняют наблюдаемую кинетику. [56]
Несмотря на очень приближенный характер этого расчета, обусловленный неопределенностью в отношении значения предэкспоненциального фактора, нет никакого сомнения в том, что величина константы скорости очень мала, и поэтому является маловероятным, что данный тип реакций может играть какую-либо существенную роль в реакциях тема или гемопротеинов. Это особенно справедливо в случае каталазы, которая не упоминалась в этом разделе, потому что все попытки приготовить ее ферро-форму оканчивались неудачей. [57]
Недавние опыты Кейлина и Хартри [ 45, с полной очевидностью показавшие, что метгемоглобин и метмиоглобин восстанавливаются, когда они реагируют с перекисью водорода в концентрации, достаточной для каталитического разложения, а также их прежние результаты [16, 17], свидетельствующие о восстановлении азид-каталазы перекисью водорода, являются бесспорным доказательством того, что для разложения перекиси с помощью гемопротеинов возможен такой путь реакции, который включает изменение валентности. Трудно, однако, предложить какой-либо механизм для реакций метгемогло-бина и метмиоглобина, потому что и здесь участвует перекисный комплекс не определенной структуры. [58]
Страницы: 1 2 3 4