Гемопротеин
Cтраница 2
Цитохром Р450 представляет собой гемопротеин, который широко используется при биологическом окислении, катализируемом оксидазами со смешанной функцией. [16]
Белок определять легко, а бактериальные гемопротеины имеют характерную хемилюминесценцию. При определении белка следует убедиться, что фоновые концентрации белков незначительны. Поскольку различные микроорганизмы содержат разные количества белка, определение этого компонента биомассы целесообразно проводить в ситуациях, когда в пробе присутствует один вид микробов. [17]
Важные стереохимические свойства железопорфирина в гемопротеинах были установлены на основе рентгеноструктурного анализа высокого разрешения модельных низкомолекулярных ме-таллопорфириновых комплексов. Эти данные были получены при подробном кристаллографическом исследовании комплексов пор-фиринов с ионами металлов, имеющими неодинаковые ионные радиусы, и железопорфириновых комплексов в различных спиновых состояниях. Для последующего обсуждения необходимо привести лишь те данные, которые относятся к стереохимии железопорфирина в гемопротеинах. Радиус центральной полости, ограниченной пиррольными атомами азота, определяется электронной структурой ядра порфина и остается практически постоянным. [18]
При изучении реакции гем-группы в гемопротеинах всегда необходимо следить за тем, чтобы никакие изменения структуры протеина не влияли на результаты. Полную денатурацию легко узнать по осаждению и флоккуляции, а также по выделению тема из гема-тина, но при этом могут происходить и менее существенные изменения. [19]
 |
Витамин B2. 280. [20] |
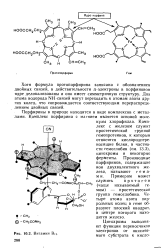
Комплекс с железом служит простетической группой гемопротеинов, к которым относятся кислородпере-носящие белки, в частности гемоглобин ( см. 13.3), цитохромы и некоторые ферменты. Производные порфиринов, содержащие ион двухвалентного железа, называют г е м а-м и. Примером может служить протогем ( чаще называемый ге-мом) - простетическая группа гемоглобина. Четыре атома азота пир-рольных колец в теме образуют плоский квадрат, в центре которого находится железо. [21]
Гем является простетической группой всего семейства гемопротеинов, наиболее известный представитель которых гемоглобин переносит кислород от альвеол легких к тканям. [22]
Хотя в общих чертах все эти четыре гемопротеина, имеющие значение для биохимии перекиси водорода-каталаза, пероксидаза, гемоглобин и мио-глобин-схожи друг с другом, все же между ними существуют и значительные различия, что объясняет неодинаковое их отношение к перекиси водорода как в самом организме, так и в экспериментальных условиях. Эти различия выражаются в неодинаковых молекулярных весах, относительных количествах составляющих аминокислот, входящих в состав белковой части молекулы, и в числе и доступности групп протопорф ирина железа, связанных с белком. Особое значение имеет то, что каталаза и гемоглобин имеют по четыре протопорфириновых группы на молекулу, тогда как пероксидаза и миоглобин несут только по одной группе. [23]
Магнитные свойства гидроксидов железо ( III) гемопротеинов и железо ( III) порфиринов сходны в том отношении, что обе группы соединений обладают пониженным парамагнетизмом. Сущность этого объяснения заключается в том, что ОН - вызывает большее расщепление поля лигандов, чем Н2О, так как известно, что аквомономеры имеют высокоспиновое состояние. [24]
Источником железа для этой реакции является ферритин, который считается резервным гемопротеином, откладывающимся в клетках костного мозга, печени и селезенки. [25]
Мессбауэровская спектроскопия цитохромов позволила получить важные сведения об особенностях строения этих гемопротеинов, обеспечивающих перенос электронов в митохондриях клетки. В первой из упомянутых работ мессбауэровский спектр цитохрома с оказался весьма похож на спектр оксигемоглобина, несмотря на то что железо в образце находилось в окисленном состоянии. [26]
Один подход к проблеме выяснения природы взаимодействия между перекисью водорода и гемопротеинами заключается в исследовании свободной группы протопорфирина железа в том или другом состоянии окисления или в комплексах. [27]
Структурные данные четко свидетельствуют о том, что стереохимические изменения железо-порфирина в гемопротеинах связаны с переходами спинового состояния центрального координированного иона металла. Однако из-за отсутствия достаточно точных стереохимических данных невозможно сделать каких-либо количественных оценок относительного вклада изменений структуры железопорфирина по сравнению с постулированным изменением длины связи Fe-Мимидазол. Несомненно, таким количественным оценкам препятствует тот факт, что дезоксигемоглобин и координированные тетрамерные гемогло-бины млекопитающих кристаллизуются в различных пространственных группах симметрии [113], вследствие чего невозможно прямое сопоставление соответствующих четвертичных структур, например, разностным методом Фурье. Кроме того, было постулировано [103, 128], что оба конформационных события носят три-герный характер и инициируют изменение четвертичной структуры при отщеплении или связывании молекулы кислорода вследствие изменений в F-спирали субъединиц белка, содержащих координирующий остаток гистидина. Предполагается, что это изменение структуры распространяется, на другие области белка. Однако природа изменений в F-спирали пока не ясна. [28]
В дополнение к таким структурным изменениям, происходящим в том случае, когда гемопротеины принимают участие в окислительно-восстановительных реакциях, имеется еще одна возможность необратимого окислительного воздействия на само порфириновое кольцо. [29]
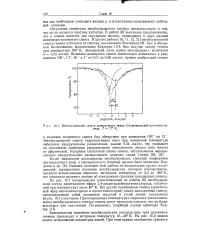 |
Мессбауэровский спектр диметилового эфира 2 4-диацетилдейтерогеминхло. [30] |
Страницы: 1 2 3 4