Геометрия - молекула
Cтраница 2
Геометрия молекулы этилена значительно проще, чем этана, так как все шесть атомов этилена лежат в одной плоскости. Энергетический барьер вращения вокруг углерод-углеродной двойной связи достаточно высок, поэтому жесткая конфигурация нарушается только при высоких температурах. [16]
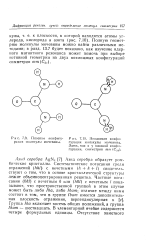 |
Плоская конфигу - [ IMAGE ] Неплоская конфи. [17] |
Полную геометрию молекулы мочевины можно найти различными методами; в разд. [18]
Из геометрии молекулы этот потенциал имеет как минимум три ямы. Для изотопически чистых метиловых групп ( СНз и СОз) из-за полной симметрии по перестановке трех атомов водорода три потенциальные ямы имеют равную глубину и равную высоту барьеров между ними. В квантовом режиме вращательное туннели-рование изотопически чистой метиловой группы является когерентным. Это означает, что три протона ( дейтерона) метиловой группы полностью делока-лизованы в трех позициях. [19]
Если геометрия молекулы приводит к необходимости или возможности-пространственного сближения двух реакционных центров, то это находит свое отражение в некоторых особенностях реакций. Это наблюдается, например, в случае реакций циклизации, приводящих к образованию устойчивых циклических продуктов; кольчато-цепной таутомерии, при которой оба тау-томера находятся в равновесии; эффекта соучастия или анхимерного содействия, когда реакция идет через промежуточное циклическое соединение, не выделяемое в свободном состоянии; при наличии пространственных затруднений. [20]
Такая геометрия молекул характерна для соединений, находящихся в газообразном состоянии. При переходе в твердое состояние геометрическое строение этих молекул резко меняется. Рассмотрим такое изменение на следующем примере. [21]
Такая геометрия молекул ожидается при рассмотрении отталкивания электронных пар валентной оболочки ( см. разд. [22]
Однако геометрия молекул не сводится к геометрии ядерных скелетов. Атомы, образующие молекулу, обладают электронными оболочками с тем или иным распределением электронной плотности. Наряду с силами притяжения между электронными оболочками атомов действуют силы отталкивания, вследствие чего атомные ядра располагаются на определенных расстояниях друг от друга. Каждому атому может быть тем самым приписан определенный радиус - так называемый атомный радиус для атомов, связанных силами валентности, и ван-дер - Ваальсов радиус для атомов различных молекул и для атомов одной и той же молекулы, непосредственно друг с другом не соединенных. Наряду с геометрией ядерного скелета существует геометрия телесной молекулы, сводящаяся к геометрии распределения электронной плотности. Соответствующие сведения дает структурный анализ свободных молекул и главным образом молекулярных кристаллов. [23]
Иногда геометрия молекул такова, что л-электронные облака перекрываются электронными облаками близлежащих a - связей. [24]
По геометрии молекулы представляют собой два полуоктаэдра с атомом серы в центре основания - квадрата - и пятью атомами фтора. [25]
Влияние геометрии молекул на их адсорбцию на ГТС при нулевом заполнении поверхности ярко проявляется не только для квазижестких молекул, но и для молекул, имеющих внутреннее вращение. Генри, несмотря на рост молекулярной массы, сильно уменьшается. Очевидно, это вызвано тем, что метальные группы в орго-положениях вызывают увеличение угла поворота бензольных колец друг относительно друга вследствие сильного отталкивания, возникающего между метильной группой в этом положении у одного кольца и атомом водорода или метильной группой в том же положении у второго кольца. У 2 2 6 6 -тетра-метилдифенила, несмотря на наибольшую в рассматриваемом ряду производных бифенила молекулярную массу, величины К оказываются наименьшими. В этом случае внутримолекулярное отталкивание двух групп СН3 в соседних положениях 2 и 2 и еще двух групп СН3 в соседних положениях 6 и 6 у разных колец приводит к почти перпендикулярному расположению бензольных колец в молекуле и резко ослабляет межмолекулярное взаимодействие этой молекулы с ГТС. [26]
Изменение геометрии молекулы при переходе одного из атомов через, плоскость, образованную тремя другими атомами, ведет к изменению конфигурации молекулы: говорят, что происходит обращение ( инверсия) конфигурации. [27]
При подходящей геометрии молекул может также проявляться взаимодействие с а-нитрогруппами. Уже было отмечено, что в ю-нитроацетофеноне нет никакого взаимодействия, а у нитрокислот [81] наблюдается повышение vCO примерно на 30 см-1 по сравнению с исходными соединениями, что было объяснено дипольным взаимодействием. Аналогично соединение I, исследованное Нейлан-дом и др. [82], имеет только одну карбонильную полосу, а соединение II характеризуется двумя полосами при 1715 и 1748 см-1, что указывает на сильный дипольный эффект. [28]
Специфика геометрии молекул ароматических соединений заключается в тенденции к копланарному расположению атомов и выравниванию длин связей в ароматическом цикле. Современные методы установления молекулярной структуры ( рентгенография и нейтронография кристаллов, газовая электронография и микроволновая спектроскопия свободных1 молекул) делают доступными геометрические параметры почти всех ароматических систем. [29]
Данные о геометрии молекул и отдельных функциональных групп были с успехом использованы для предсказания геометрической конфигурации различных молекул, анализа пространственных препятствий и напряжений валентных углов в молекулах. [30]
Страницы: 1 2 3 4