Геометрия - переходное состояние
Cтраница 1
Геометрия переходного состояния 16 вблизи реакционного центра имеет много общего с геометрией стабильных димеров карбоновых кислот. Это подобие наводит на мысль, что в реакциях, сходных с мутаротацией, карбоно-вые кислоты могут образовывать переходные состояния с относительно низким стандартным потенциалом, В таких переходных состояниях карбонильный кислород кислоты принимает протон от одного положения молекулы субстрата, а гидроксильная группа кислоты предоставляет протон другому положению. И действительно, для мутаротации глюкозы в бензольных [34] или нитромета-новых [35] растворах карбоновые кислоты - значительно более эффективные катализаторы, чем фенолы с той же кислотностью. Несомненно, что в водных растворах такие переходные состояния менее важны, так как вода способна быть и донором, и акцептором протона. Окси-пиридин ускоряет мутаротацию глюкозы в водном растворе только в 4 - 5 раз сильнее, чем можно было ожидать из его кислотных и основных свойств. [1]
По-видимому, геометрия переходного состояния при адсорбции та же, что и для я-комплекса олефина, в котором его структура, вероятно, лишь незначительно искажена по сравнению со структурой изолированного алкена. [2]
Большинству читателей известна геометрия переходного состояния для случая нуклеофильного замещения ( 5м2 - реакция) при тетраэдрическом атоме углерода. [3]
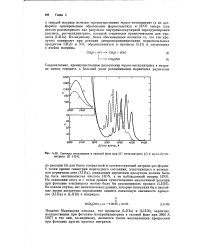 |
Спектры поглощения в газовой фазе при 25 метилнитрита ( 1 и mpem - бутил-нитрита ( 2. [4] |
С точки зрения геометрии переходного состояния, участвующего в возможном первичном акте ( ЫПа), ожидаемым первичным продуктом должна была бы быть азотноватистая кислота HON, а не наблюдаемый изомер HNO. Во всяком случае, нет окончательных данных, которые позволили бы в настоящее время достаточно определенно оценить возможную значимость процессов ( ЫПа) и ( ЫПб) в матрицах. [5]
Этот факт указывает, что геометрия переходного состояния сильно зависит от стабильности соединения. III и получил оптически активное вещество. [6]
При перегруппировке Вагнера - Меервейна геометрия переходного состояния, вероятно, изменяется от системы к системе в зависимости от немигрирующих заместителей у конца и начала миграции. [7]
При оценке влияния заместителей на геометрию переходного состояния необходимо изучать реакционные серии, в которых меняются заместители не только в субстрате, но и в нуклеофиле. Для процессов б1 / / 2 такие перекрестные серии изучены, кроме серий с бензилгалогенидами, лишь в случае Х - бромкетонов. [8]
 |
Рассчитанные зшачешша эшергшш актшвацшш ( кДж / моль для некоторых реакций. [9] |
Наибольший интерес вызывает вопрос о точности вычисления геометрии переходного состояния и Еакт квантово-химическими методами. [10]
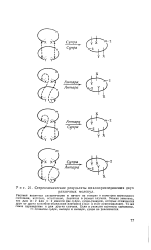 |
Стереохимические результаты циклоприсоединения двух различных молекул. [11] |
Рисунки являются схематичными и ничего не говорят о геометрии переходного состояния, которая, естественно, различна в разных случаях. То же самое справедливо и для других случаев. Если в реакции партнеры одинаковы, то процессы супра, антара и антара, супра не различаются. [12]
Приведенные изображения весьма схематичны и ничего не говорят о геометрии переходного состояния, которое, естественно, может быть различным в каждом случае. [13]
При подобного рода расчетах основная неточность ( при условии, что геометрия переходного состояния приближенно известна, как это имеет место в данном случае) обусловлена трудностью выбора надлежащих выражений для энергии, как функции положений групп, приближаемых друг к другу в процессе реакции. Такие данные получаются из спектроскопических значений энергий растяжения и изгиба связей, а также значений сжимаемости атомов и групп молекул - часто вычисляемых по вириальным коэффициентам простых газообразных веществ. Хорошее согласие между теорией и экспериментом в примере, изученном Ригером и Вестхеймером ( см. выше), свидетельствует об обоснованности сделанных в этой работе приближений и допущений. [14]
Повышенная реакционная способность нитроциклобутана объясняется авторами не напряжением четырехчленного цикла, а геометрией переходного состояния, благоприятной для атаки водородного атома. [15]
Страницы: 1 2 3 4