Четырехвалентный германий
Cтраница 3
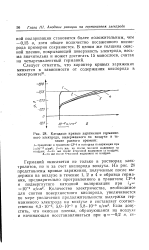 |
Катодные кривые заряжения германиевого электрода, выдержанного на воздухе в течение разного времени. [31] |
В целом же толщина окис-ной пленки, покрывающей поверхность электрода, весьма значительна и может достигать 15 монослоев, считая на четырехвалентный германий. [32]
Хотя катионы германия существуют в растворах наряду с анионами, начиная с рН 7 и ниже 38, 57 ], соли четырехвалентного германия почти не известны. Примером их служит сульфат германия Ge ( SO4) 2, получающийся нагреванием тетрахло-рида с серным ангидридом при 160 в автоклаве. Легко гидролизу-ется водой, а при нагревании разлагается. [33]
Такие примесные полупроводники называются избыточными электронными полупроводниками, а их избыточная электронная проводимость называется электронной или типа п ( negative - отрицательный), например четырехвалентный германий с примесью пятивалентного мышьяка. [34]
Соединения четырехвалентного германия легко гидролизуются и обладают некоторыми свойствами, похожими на свойства соответствующих соединений четырехвалентного олова; однако последние легче восстанавливаются. Для четырехвалентного германия соли кислородных кислот не характерны, а галогениды имеют выраженную-тенденцию к образованию аддуктов. Моногерман, тетрагалогениды, алкильные и арильные производные германия являются ковалент-ными соединениями. [35]
Рассмотрим механизм образования зарядов, воспользовавшись снова плоскостной моделью кристаллической решетки. Если в четырехвалентный германий добавить пятивалентное вещество, например сурьму, то пятивалентный атом сурьмы четырьмя валентными электронами образует ковалентную связь с четырьмя соседними атомами германия, а пятый валентный электрон атома сурьмы остается лишним и может быть достаточно легко отделен от атома. Такие полупроводники обладают электропроводностью п-типа. Примеси, которые отдают исходному полупроводнику свои электроны, называют донорными. [36]
Солеоб-разные соединения четырехвалентного германия - сульфат, ацетат и ди-гидрофосфат - получаются лишь в безводных условиях и полностью гид-ролизуются водой. [37]
Германий, наряду с кремнием, широко применяется для изготовления полупроводниковых диодов и триодов. Добавляя к четырехвалентному германию в качестве донорной примеси в ничтожном количестве пятивалентный мышьяк или сурьму, мы получим полупроводник, в кристаллической решетке которого пятый электрон связан слабее с ядром. [38]
Концентрация носителей тока в полупроводниках в очень сильной степени зависит от наличия примесей. При введении в четырехвалентный германий Ge или кремний Si элементов пятой группы периодической системы Д. И. Менделеева ( As, Sb, P и др.) пятый электрон внешней оболочки примесного атома не участвует в образовании ковалентных связей с четырьмя соседними атомами Ge и ведет себя как свободный электрон в поле кристаллической решетки. При введении же элементов третьей группы ( В, Al, Ga, In и др.), которые входят в Ge как примеси замещения, в соответствующем узле решетки для насыщения четырех ковалентных связей нехватает одного электрона. [39]
В настоящее время стало известным, что некоторые осадочные железные руды содержат повышенные количества германия и могут служить источнико м его получения. С другой стороны, четырехвалентный германий близок по величине ионного радиуса к. [40]
Простые некомплексованные ионы двухвалентного германия Ge2 в водных растворах не существуют. Допускается, что при восстановлении четырехвалентного германия простые ионы Ge2 появляются как промежуточная ступень, а затем моментально происходит, в зависимости от условий, их гидролиз, комплексование или диспропорционирование. При прокаливании соединений четырехвалентного германия с углеродистыми или серусодержащими веществами могут образоваться относительно легколетучие окись или моносульфид германия. Температура возгонки окиси германия равна 710, моносульфида ( начало возгонки) 430, при температуре выше 650 моносульфид улетучивается полностью. [41]
Возможно также применение для этих целей электролитов, содержащих германий в двухвалентной форме. Известно [306], что в противоположность соединениям четырехвалентного германия его двухвалентные соединения легко восстанавливаются до металла на капающем ртутном катоде. [42]
Выше 550 С идет обратная реакция. Из растворов GeO может быть получена восстановлением соединений четырехвалентного германия металлическим цинком или фосфорноватистой кислотой. Свежеосажденная GeO может иметь различную окраску: от желтой до красной, очень мало растворима в воде, легко растворима в галогеноводородных кислотах и слабо растворима в щелочи. [43]
Схема Тарнера имеет ряд недостатков. По Тарнеру, поверхность электрода покрыта монослоем окислов четырехвалентного германия. В действительности состав окис-ной пленки зависит от потенциала и времени анодной поляризации и может достигать нескольких монослоев. Это означает, что в процессе анодного растворения германия происходит более глубокое окисление поверхности, и оно определяется не только величиной поляризующего тока, но и продолжительностью растворения. [44]
Сульфосоли германия хорошо растворимы в воде. При под-кислении сульфосоли разрушаются и выпадает белый осадок сульфида четырехвалентного германия. [45]
Страницы: 1 2 3 4