Герцфельда
Cтраница 3
В нижней части табл. 26 приведены энергии решетки для некоторых неизвестных соединений, которые по заключению Гримма и Герцфельда ( Grimm, Herzfeld, 1923) были вычислены при допущении, что эти соединения, если бы они существовали, должны были образовывать такую же решетку, как и аналогичные им известные соединения. Из полученных таким образом сильно отрицательных величин сродства образования видно, что такие соединения, как XeF nNaF2, не могут существовать. [31]
В нижней части табл. 26 приведены энергии решетки для некоторых неизвестных соединений, которые, по заключению Гримма и Герцфельда ( Grimm, Herzfold, 1923), были вычислены при допущении, что эти соединения, если бы они существовали, должны были образовывать такую же решетку, как и аналогичные им известные соединения. [32]
В настоящее время для Е приняты, величины, указанные в работе Лейдлера [45], а не величины Раиса и Герцфельда. [33]
А, соединенным с СО2; &, по существу, является средним коэффициентом поглощения исследуемого образца. Множитель п в механизме Франка - Герцфельда равен 1; однако k I при стационарном состоянии не превышает ] / 8 общей скорости поглощения. [34]
Поскольку полный анализ промежуточных и конечных продуктов не производился и значение констант образования этих продуктов не установлено, невозможно дать хотя бы качественные оценки механизма процесса. Можно считать лишь установленным, что обычная цепная неразветвленная схема крекинга углеводородов Раиса - Герцфельда при температурах плазменного процесса неприменима. [35]
Гомогенный случай, при котором превращение мицелл или молекул в другие идет непрерывно, путем образования смешанных кристаллов. Этот случай тождествен с разобранной выше реакцией между нитроализарином и солью, и по Герцфельду он будет следовать закону действующих масс гомогенной реакции. [36]
Измеренные концентрации радикалов в зоне распада С2Н6 и С3Н8 значительно превышали равновесные концентрации в реакциях Н2 - t 2Н или СН4 Г - СН3 Н при температурах крекинга, что является прямым доказательством участия радикалов в процессе. Однако указанное расхождение между вычисленной и экспериментальной концентрациями радикалов свидетельствует о том, что радикально-цепные схемы Раиса и Герцфельда не описывают реального крекинга. [37]
Элтентон на основании масс-спектрометрических измерений показал, что действительно метальные радикалы образуются из этана по реакции второго порядка. Далее современные данные относительно скоростей элементарных реакций позволяют заключить, что энергия активации всего процесса, рассчитанная на основе механизма Раиса и Герцфельда ( расчет велся по уравнению ( 39), стр. [38]
Кроме того, изучение реакции замещения атомов дейтерия с молекулами метана и этана показало [367, 368], что для энергии активации в первоначальных радикально-цепных схемах Раиса и Герцфельда были приняты слишком завышенные значения. [39]
САХАРОЗА, тростниковый сахар, свекловичный сахар С Н Оц, полисахарид ( см. Полисахариды) весьма, распространенный в растениях ( в листьях, плодах, корнях и пр. Герцфельду выражается следующей эмпирич. [40]
Полисахариды), весьма распространенный в растениях ( в листьях, плодах, корнях и пр. Герцфельду выражается следующей эмпирич. [41]
Этот вопрос был вновь исследован теоретически и экспериментально Лейдлером и Войцеховским. С помощью теории мономолекулярных реакций они показали, что в условиях эксперимента инициирование, действительно, должно идти по второму порядку. Поэтому следует принять механизм Кюхлера и Тейле, тем более что, как было показано, этот механизм приводит к более точной сходимости значений энергии активации и предэкспоненциального множителя, чем это следует из механизма Раиса - Герцфельда. [42]
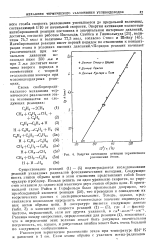 |
Энергия активации реакции термического разложения этана. [43] |
Существование реакций ( 1) - ( 4) подтверждается исследованиями реакций указанных радикалов фотохимическими методами. Следующие шесть этапов обрыва цепи в этом отношении представляют собой более трудную проблему. Нельзя решить ни одно уравнение скорости, не упростив механизм до одного или максимум двух этапов обрыва цепи. В оригинальной схеме Раиса и Герцфельда было произвольно допущено, что преобладающей является реакция ( 56), что приводило к совпадению их теоретических данных с экспериментальными. Теперь, однако, представляется возможным определить относительное значение индивидуальных актов обрыва цепи. Разница между скоростями, определенными для реакции ( 4), показывает, что в определении этих величин может быть допущена значительная погрешность, по, однако, и допустимая ошибка может быть очень большой по следующим соображениям. [44]
В действительности, например, при адиабатном процессе, когда Q 0, сумма ZNidsi не равна нулю и, стало быть, не означает элемента тепла. При адиабатном процессе указанная сумма в простейших случаях определяет прирост молекулярно-кинетической энергии, но и это не всегда имеет место, так как, например, при воздействии на молекулярное поле перераспределение молекул по фазовым ячейкам приводит к изменению не только молекулярно-кинетической, но также и молекулярно-потенциальной энергии. Упомянутое освещение формулы (2.3) не приводит Герцфельда к ошибочным выводам потому - - что в последующем он рассматривает только изотермические приложения формулы. [45]
Страницы: 1 2 3 4