Гетероатома
Cтраница 2
Гетероатомы ( кислород, сера, азот), содержащиеся в асфальтеновых молекулах в относительно небольшом количестве по отношению к количеству углеродных атомов, не изменяют в значительной степени основу этих тел ( углеродный скелет), но они увеличивают разнообразие структурных элементов. Некоторые гетероатомы могут образовывать с углеродными атомами гетероциклы или входить в состав различных функциональных групп, придавая специфический химический характер некоторым группам поликонденсированных комплексов. [16]
Гетероатомы ( О, S, N) могут входить как в боковые цепочки, так и в состав кольчатых структур. [17]
Гетероатомы, например азот, кислород, сера и кремний, иногда рассматривают при образовании названий как составляющие часть углеродного скелета. Скелет называется так, как если бы гетероатом был углеродом, и специальное слово вместе с номером ставится перед названием. Такой способ очень полезен в наименовании сложных структур, которые иначе потребовали бы названия и нумерации двух или более сложных групп. [18]
Гетероатомы располагаются в алфавитном порядке. Каждая молекулярная формула повторяется столько раз, сколько она содержит гетероатомов. HAIC Index является вспомогательным указателем к Formula Index и позволяет установить, Какие молекулярные формулы с соответствующими гетероатомами в нем приведены. [19]
Гетероатомы ( азот, сера, кислород и др.) могут иметь различные степени окисления. Восстановители позволяют понизить степень окисления ге-тероатомов. Однако механизм этих превращений изучен меньше, чем механизм реакций восстановления, затрагивающих атом углерода. Степени окисления гетероатомов в основных функциональных группах перечислены в табл. 18.2. Реакцией, наиболее важной в этой группе, является восстановление ароматических нитропроизводных в амины: металлами в кислой среде ( Fe, Zn), солями-восстановителями ( FeSO4, SnCl2), производными серы [ Na2S, ( NH4) 2S ] или каталитически в присутствии никеля и платины. [20]
Гетероатомы ( азот, сера, кислород и др.) могут иметь различные степени окисления ( разд. Показанные в табл. 19.2 превращения соответствуют реакциям окисления; их механизм не всегда точно выяснен, однако часто наблюдаются реакции электрофильного характера. [21]
Гетероатомы указывают по а-системе. [22]
Гетероатомы должны получить наименьшие номера в соответствии табл. I ( стр. [23]
Гетероатомы, входящие в состав цикла, оказывают влияние на свойства гетероциклических соединений. В гетероциклах в отличие от молекулы бензола, как правило, наблюдается неравномерное распределение л-электронной плотности. Например, в пятичленных гетероциклах ( в фуране, тиофене и пирроле) электронная плотность смещена от гетероатома в сторону кольца и максимальна в а-положениях. [24]
Гетероатомы, включенные в молекулу комплексонов, выступают в качестве дополнительных координационных партнеров, также способствуя упрочнению комплексов. [25]
Гетероатомы ( атомы элементов, отличных от элемента, атомы которого преобладают) также могут быть включены в нашу схему с помощью формулы Шеннона. Разметка молекулярного графа таким образом, чтобы ранее эквивалентные вершины становились неэквивалентными, увеличивает величину С ( т), так как прежде эквивалентные связки по необходимости становятся неэквивалентными. С другой стороны, величина С ( ч) не изменяется, когда метка не влияет на классы эквивалентности связок. Предостережением против одновременного суммирования числа сложностей или числа индексов является тот факт, что если это осуществить, то отдельные величины исчезают из виду в этой сумме, и на основании полученного таким образом числа нельзя сказать, присутствуют гетероатомы или же нет. [26]
Электроотрицательные гетероатомы ускоряют металлирова-пне в гем-положенпс за счет делокализацпи заряда. В этих случаях осложнения могут происходить из-за карбеноидного а-элиминирования ( см. с. В примерах 12 и 13 табл. 15.1.1 гетероатомы недостаточно электроотрицательны, и причины активации не ясны. [27]
Гетероатомами являются кислород, сера или азот. [28]
Такие гетероатомы входят в состав разнообразных функциональных групп: ОН, NH2) СО, SO, РО и др. ЛСР-хелаты являются жесткими льюисовыми кислотами. В соответствии с принципом жестких и мягких кислот и оснований ( ЖМКО), они хорошо реагируют лишь с жесткими основаниями. К мягким основаниям относятся меркаптаны, сульфиды, фосфины, галогениды-они не реагируют с ЛСР-хелатами. Практически не взаимодействуют с ЛСР фуран, тиофен, пиррол и их нефункциональные производные, а также нитрилы, нитросоединения, галогенопро-изводные и углеводороды. В качестве растворителей в экспериментах с ЛСР-хелатами используют СС14, CDC13 и CS2, с ЛСР-солями - воду и ацетон. Одним из наиболее активных субстратов в реакциях с ЛСР-хелатами является вода, поэтому исследуемые препараты, в том числе растворители, нужно тщательно обезвоживать. Для удаления воды Ей ( ДПМ), возгоняют в вакууме. [29]
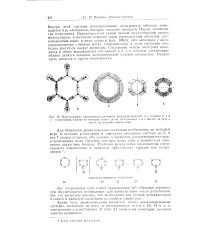 |
Молекулярные электронные состояния молекулы бсн. чола. а - i-спязи. б, в и г - - я-состояния, каждое и. ( которых занято днумн электронами. и г богаче энергией. [30] |
Страницы: 1 2 3 4