Гибель - радикал
Cтраница 3
При стационарном состоянии скорость гибели радикалов на стенках должна равняться общей скорости зарождения радикалов в объеме плюс общая скорость разветвления. [31]
При диффузионном обрыве скорость гибели радикалов на стенке велика и вероятность прилипания атома к стенке близка к единице. Скорость обрыва цепи лимитируется диффузией атома или радикала к стенке. [32]
При стационарном состоянии скорость гибели радикалов на стенках должна равняться общей скорости зарождения радикалов в объеме плюс общая скорость разветвления. [33]
 |
Термографические кривые 25 ( 1 и 98 % - ных ( 2 растворов Й202.| Фазовая диаграмма Н20 - Н202. [34] |
Полученные результаты о связи быстрой гибели радикалов с фазовым переходом заставили нас предположить, что радикалы в изучаемой системе могут существовать и при температурах выше температуры фазового перехода. [35]
Суммарная скорость реакций зарождения и гибели радикалов входит в систему кинетических уравнений в виде уравнения баланса между источниками и стоками радикалов и определяет общую скорость процесса. [36]
Здесь следует заметить, что гибель радикала Н02 на стенке существенно зависит от материала, из которого стенка сделана. Для некоторых материалов гибнут все радикалы, достигшие стенки, для других - значительная часть отражается обратно в объем сосуда без изменений. [37]
Подобны также кривые зависимости скорости гибели радикалов от времени выдержки при комнатной температуре. Эти радикалы довольно быстро исчезают в течение первых двух часов, а после 10 часов остаются радикалы, которые исчезают чрезвычайно медленно и еще могут наблюдаться в концентрациях ( 0 05 - 0 1) - 1017 1 / г даже через полтора месяца после облучения. В нагретых до 50 С образцах скорость исчезновения радикалов возрастает в 10 раз по сравнению с комнатной температурой, причем приблизительно сохраняется экспоненциальный закон спада концентрации радикалов от времени выдержки, который наблюдается и при комнатной температуре. [38]
Следует подчеркнуть, что кинетика гибели радикалов в большой мере определяется физическими свойствами матрицы. [39]
Большие ошибки при измерениях скоростей гибели радикалов приводят к тому, что значения, полученные в различных лабораториях, отличаются друг от друга в лучшем случае лишь в 2 раза. [40]
Однако имеются косвенные указания на частичную гибель радикалов. [41]
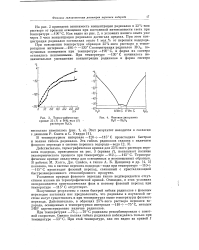
На рис. 1 и 2 представлены кинетические кривые гибели радикалов I и II при разных температурах. При промежуточной температуре 35 С наблюдается смешанный механизм, как видно из кривых. [42]
Предложенные данные, показывающие независимость скорости гибели радикалов от жесткости системы в момент размораживания движения сегментов и сравнительно интенсивное взаимодействие оставшихся радикалов, несмотря на значительное расстояние между ними, равное сотням и более ангстрем, позволяют сделать заключение, что процессы гибели радикалов при увеличении колебательного движения звеньев системы в очень малой степени идут в результате непосредственной рекомбинации радикалов за счет сближения радикалсодержащих сегментов. По-видимому, увеличение подвижности звеньев дает начальный толчок процессам гибели ближайших радикалов. [43]
 |
Зависимость скорости неразветвленной реакции от времени т. [44] |
Обрывом цепей на стенке за счет гибели радикалов О и ОН, а также продолжением цепей за счет образовавшегося радикала НО2 можно пренебречь, так как атомов кислорода и гидроокиси в реакции накапливается значительно меньше, чем атомов водорода. Радикал НО2 при малых давлениях не активен. [45]
Страницы: 1 2 3 4