Гибель - цепь
Cтраница 2
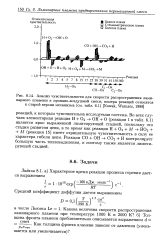 |
Анализ чувствительности для скорости распространения ламинарного пламени в пропано-воздушной смеси. номера реакций относятся к старой версии механизма ( [ Nowak, Warnatz, 1988 ]. [16] |
Во всех случаях элементарная реакция Н 02 - ОН О ( реакция 1 в табл. 6.1) является ярко выраженной лимитирующей стадией, поскольку это стадия развития цепи, в то время как реакция Н СЬ М - НС2 М ( реакция 15) имеет отрицательную чувствительность в силу ее характера гибели цепи. Реакция СО ОН - 4 СОг Н контролирует большую часть тепловыделения, и поэтому также является лимитирующей стадией. [17]
В то же время энергии активации реакций обрыва цепей обычно близки к нулю, и поэтому константы скорости обрыва цепей мало зависят от природы свободного радикала. Поэтому отношение скоростей гибели цепи на различных свободных радикалах wT1 / wr2 определяется в первую очередь отношением концентраций этих свободных радикалов и, следовательно, как правило, сильно отличается от единицы. [18]
Оказалось, что инициирование происходит практически мгновенно и весь катализатор переходит в активные центры. Затем за счет реакции гибели цепи концентрация активных центров медленно понижается. [19]
Для давлений выше 100 мбар ( для той же температуры 800 К) воспламенения не наблюдается. Второй предел воспламенения обусловлен конкуренцией процессов разветвления цепей и гибели цепей в газовой фазе. [20]
Над вторым пределом положение меняется. Таким образом, чем выше давление, тем реже реакция ( 6) приводит к гибели цепи. [21]
Рассмотрим механизм регулирующего действия солевых катализаторов. Соотношение между продуктами в этом случае всецело определяется реакциями продолжения цепи и не зависит от зарождения и гибели цепей. [23]
В данном звене цепи расходуется одна молекула исходного вещества. Поэтому число молекул, расходующихся в результате образования в стадии инициирования радикала, равно числу звеньев цепи, осуществляемых от инициирования до гибели цепи, называемому длиной цепи. [24]
Когда давление повышается и становится больше определенного значения ( первый предел воспламенения), наблюдается спонтанное воспламенение, так как приведенная скорость диффузии радикалов к стенке реакционного сосуда ( D оср 1), на которой они гибнут, становится меньше скорости образования радикалов в газовой фазе. Первый предел воспламенения сильно зависит от химической природы поверхности реакционного сосуда, поскольку этот предел есть результат конкуренции одновременно протекающих процессов разветвления цепей в газовой фазе и гибели цепей на поверхности. На такую чувствительность к материалу поверхности указывает то обстоятельство, что различным материалам стенки реакционного сосуда ( например, стекло, железо, медь, палладий) отвечают различные пределы воспламенения. [25]
Большой активностью обладает также безводная HClQj. По мнению авторов, хлорная кислота и ацетилперхлорат обладают двумя преимуществами, которые делают их сильными инициаторами полимеризации: катионы Н или СНзС 0 способны вести быструю реакцию, а анион СЮ4 практически не участвует в гибели цепи, поскольку он имеет слабо выраженные основные свойства. Предполагается, что низкая активность А1С1з и SbFs зависит от медленной реакции инициирования. Если катализатор полимеризации долго не удаляется из реакционной системы, наблюдается распад уже образовавшихся молекул полимера. [26]
С повышением давления воспламенение продолжает происходить до тех пор, пока скорость разветвления больше скорости объемной гибели цепи. Как только давление достигает значения, при котором скорость обрыва цепи становится больше скорости разветвления, реакция останавливается. Второй предел соответствует такому давлению реагирующей смеси, при котором скорости разветвления и объемной гибели цепей равны. [27]
Было отмечено, что &2 и &4 имеют относительно нормальные величины предэкспоненциальных множителей, тогда как для k1 эта величина существенно отклоняется от обычных значений. Большая величина предэкспоненциального множителя для k1 указывает на весьма беспорядочное переходное состояние, которое очень легко представить себе в виде клетки, содержащей больше чем одну пару радикалов, возможно, образовавшихся не из одной, а из разных полимерных цепей. Энергия активации термического инициирования согласуется с представлением о том, что радикал выходит из клетки в резулыате гибели цепи. Можно было, конечно, ожидать, что оба процесса термического инициирования конкурируют друг с другом в соответствии с их относительной энергетикой. [28]
Обсудим возможный механизм регулирующего действия солевых катализаторов. В катализированном окислении циклогексана спирт и кетон образуются и расходуются цепным путем ( см. гл. Соотношение между ними в этом случае должно всецело определяться реакциями продолжения цепи и не зависеть от зарождения и гибели цепей. Изменить соотношение концентраций спирта и кетона можно только путем воздействия на реакции продолжения цепи. [30]
Страницы: 1 2 3