Тетраэдрическая гибридизация
Cтраница 2
Мы видели, что кристаллическая структура алмаза определяется в значительной степени тетраэдрической гибридизацией орбиталей sp3; это подтверждается тем, что межатомное расстояние в алмазе 1 54 А почти такое же, как в молекуле этана и в более тяжелых углеводородах. [16]
Подобное суммирование показывает, что такие электронные тяжи направлены к четырем вершинам тетраэдра, поэтому такая линейная комбинация называется тетраэдрической гибридизацией. В метане используется такая же гибридизация для образования четырех cr - связей с четырьмя атомами водорода. [17]
Подобное суммирование показывает, что такие электронные тяжи направлены к четырем вершинам тетраэдра, поэтому такая линейная комбинация называется тетраэдрической гибридизацией. В метане используется такая же гибридизация для образования четырех ст-связей с четырьмя атомами водорода. [18]
Можно представить, что замещение Z на А - может протекать таким образом, что за время этого процесса углерод будет сохранять тетраэдрическую гибридизацию. В этом случае А - будет перекрываться с той же хр3 - гибридной орбиталью, которая связывает группу Z с углеродом. Однако такой подход группы А не очень облегчен, поскольку он допускает лишь относительно слабое одновременное перекрывание двух групп с одной и той же орбиталью углерода. Переходное состояние в действительности требует изменения гибридизации орбиталей углерода от тетраэдрической в тригональную, так что группа GR3 становится планарной и каждая из связей С - R образуется р2 - гибридом. Уходящая группа отходит из одной петли / j - орбитали, перпендикулярной плоской группе CR3, в то время как нуклеофил синхронно внедряется в другую петлю этой же орбитали. [19]
Можно представить, что замещение Z на А - может протекать таким образом, что за время этого процесса углерод будет сохра-нять тетраэдрическую гибридизацию. В этом случае А - будет перекрываться с той же зр3 - гибридной орбиталью, которая связывает группу Z с углеродом. Однако такой подход группы А не очень облегчен, поскольку он допускает лишь относительно слабое одновременное перекрывание двух групп с одной и той же орбиталью углерода. Переходное состояние в действительности требует изменения гибридизации орбиталей углерода от тетраэдрической в тригональную, так что группа CRS становится пленарной и каждая из свя-эей С - R образуется зр2 - гибридом. Уходящая группа отходит из одной петли р-орбитали, перпендикулярной плоской группе CR3, в то время как нуклеофил синхронно внедряется в другую петлю этой же орбитали. [20]
Как было указано выше, в ходе дискуссии об особенностях строения окиси этилена и циклопропана было признано, что атомы углерода в молекуле окиси этилена имеют не тетраэдрическую гибридизацию валентных электронов, а близкую к тригональной, подобной той, что имеется у атомов углерода в молекуле этилена. [21]
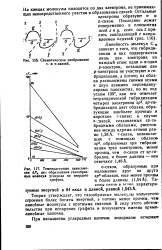 |
Схематическое изображение ч - в к-связей.| Температурные зависимости ДРН пял образования газообразных молекул углерода из твердого графита. [22] |
Линейность молекул С зависит о того, что гибридизации в них подвергаются лишь два электрона на каждый атом: один s - и один р-электрон, остальные два р-электрона не участвуют в гибридизации, а потому их облака расположены своими осям в двух взаимно перпендикулярных плоскостях, но не под углом 109, как это отвечает тетраэдрической гибридизации четырех электронов sps. [23]
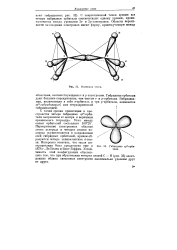 |
Молекула этапа.| Гибридные ра-орби-тали. [24] |
Гибридные орбитали дают большее перекрывание, чем чистые s - и р-орбитали. Гибридизация, включающая в себя s - орбиталь и три р-орбитали, называется зр3 - гибридизацией или тетраэдрической гибридизацией. [25]
Отсюда неизбежно уменьшение степени перекрывания орбиталей углеродных атомов. Но в рассмотрении Коулсона - Моффита для циклопропана рассматривается модель несколько лучшая, чем та, для которой принимается тетраэдрическая гибридизация углерода нормального типа. [27]
Углы, образуемые простыми связями двухвалентного кислорода, зависят от природы других атомов, связанных с кислородом. В ациклических насыщенных простых эфирах ( СН3) 20 и ( С2Н5) 20 углы С - О - С близки к тетра-эдрическим, что указывает на тетраэдрическую гибридизацию атома кислорода. Очевидно, сопряжение свободной пары атома кислорода требует, чтобы этот атом перешел в тригональное гибридизованное состояние. Связи С - О в этом соединении гораздо менее устойчивы, чем С - 0-связи ациклических простых эфиров, и, по-видимому, так же, как в случае связи С - С циклопропана, С - 0-связи образуются с участием изогнутых МО и характеризуются некоторой степенью делокализации электронов в плоскости кольца. Так, молярная восприимчивость 1 2-эпоксиэтана на 8 6 единицы превосходит аналогичную величину для уксусного альдегида ( ср. [28]
Несколько лет назад Уэланд [65] подробно рассмотрел модель XV для переходного состояния реакции элек-трофильного замещения, в которой атакующая частица ( Е) и замещаемый протон одновременно связаны с атомом углерода кольца, который приобрел тетраэдрическую гибридизацию. [29]
На основании приведенных выше примеров очевидно, что для илидного атома углерода нельзя предположить тригональ-ной гибридизации. Такой случай, вероятно, имеет место, когда карбанион способен делокализовать свой заряд за счет заместителей в результате обычного р - р л-перекрывания орбиталей. Если нет такого взаимодействия, то для орбиталей карбанионного углерода возможна тетраэдрическая гибридизация. [30]
Страницы: 1 2 3
