Гидрат - кислота
Cтраница 1
Гидраты полиборгидридных кислот очень гигроскопичны; при разбавлении их водой, выделяется много тепла, что иногда приводит к разложению. Энергично, со взрывом реагируют с концентрированными серной и азотной кислотами. По силе H2Bi0Hi0 и H2Bi2Hi2 сравнимы с серной кислотой. [1]
Формулы гидрата кислоты ( водной кислоты) и солей Зинин изображает по старинке ( см. примечание 3 на стр. [2]
Нитрониумнерхлорат и гидрат перхлорной кислоты были разделены фракционной кристаллизацией из нитрометана. Идентичность нитро-ниумперхлората была доказана при помощи спектров комбинационного рассеяния, которые полностью совпадали со спектрами ионов нитро-ниума и перхлората. [3]
Рентгеноструктурные исследования [377] гидрата ацетогид-роксамовой кислоты ( 128) [ указаны длины связей ( в нм) и валентные углы ] показывают, что атомы С-1, С-2, N и 0 - 2 лежат в одной плоскости, а атом 0 - 1 находится на расстоянии 0 0056 нм от этой плоскости. Длины связей и валентные углы в остатке RC ( 0) N очень близки аналогичным величинам у амидов [ ср. [4]
Такую очистку повторяют дважды: гидрат кислоты сушат затем в эксикаторе над. КОН и концентрированной серной кислотой ( см. разд. Кристаллы имеют вид бесцветных, иризм. [5]
Хлорокись фосфора образуется - действуя РС15 на гидраты кислот ( щелочи разрушают хлорокись фосфора) - по типу: PCI3 - - 1 - RHO РОС13 RC1 - f - НС1, где RHO есть кислота. Реакция идет по этому равенству с одно-основными кислотами, но тогда RC1 летуча и потому получается смесь RCI с РОС13 - двух летучих тел, иногда не разделяемых перегонкою. Так, действуя РС15 на борную или щавелевую кислоту, и приготовляют хлорокись фосфора. [6]
Результаты Ричардса и Смита [19] по ЯМР-спектрам гидратов кислот, обсуждавшиеся выше, приводят к выводу, что ион Н3О имеет треугольную довольно плоскую пирамидальную структуру с расстоянием между протонами 1 72 0 02 А. [7]
При нагревании [21] а, а-дихлорметилового эфира с гидратом пентаацетилглюконовой кислоты в течение 1 ч при 70 С хлоран-гидрид получен с количественным выходом. [8]
Таким образом, по данным анализа вещество это представляет как бы полуводный гидрат изобутилфосфиновой кислоты. Это тем более удивительно, что кислота многократно была перекристаллизована из совершенно сухих эфира и лигроина, а перед анализом была высушена в вакуум-эксикаторе до постоянного веса. [9]
Так как при всех реакциях между спиртами и кислотами пыделяется вода, то очевидно, что и оксониевые гидраты кислот также могут принимать участие в ходе превращения. В тех случаях, когда в продуктах реакции образуются простые эфиры, их оксониевые соединения как с кислотами, так и с галоидгидринами и серновинными кислотами также должны играть роль. [10]
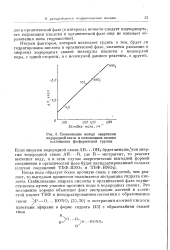 |
Соотношение между энергиями. [11] |
Когда вода образует более прочную связь с кислотой, чем реагент, то выгодным процессом оказывается экстракция гидрата кислоты. Стабилизация гидрата кислоты в органической фазе осуществляется путем участия протонов воды в водородных связях. [12]
 |
Группировки протон - вода в гидратах. [13] |
Как и в структурах ряда гидратов солей, часть воды может быть не связана с катионами; существуют гидраты кислот, в которых некоторые из молекул воды не включаются в протонированные группировки. [14]
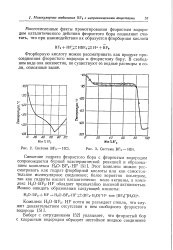 |
Система BF3 - НВг. [15] |
Страницы: 1 2 3