Гидрат - кислота
Cтраница 2
Этот комплекс можно рассматривать как гидрат фторборной кислоты или как самостоятельное молекулярное соединение; более вероятно последнее, так как гидраты кислот каталитически мало активны, а комплекс H20 - BF3 - HF обладает чрезвычайно высокой активностью. [16]
Полученный комплекс можно рассматривать как гидрат фторборной кислоты или как самостоятельное молекулярное соединение; более вероятно последнее, так как гидраты кислот каталитически мало активны, а комплекс H20 - BF3 - HF чрезвычайно активен. [17]
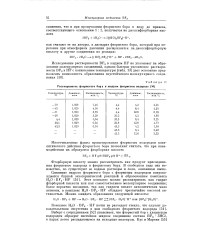 |
Растворимость фтористого бора в жидком фтористом водороде. [18] |
Этот комплекс можно рассматривать как гидрат фторборной кислоты или как самостоятельное молекулярное соединение; более вероятно последнее, так как гидраты кислот каталитически мало активны, а комплекс Н20 BF3 HF обладает чрезвычайно высокой активностью. [19]
Эти результаты считают свидетельством того, что полимеризация в среде полярного нитробензола катализируется дигидратом хлорида олова или его эквивалентами ( например, гидратом трихлороловянной кислоты SnCl3OH - H2O), а в среде неполярного четыреххлористого углерода - моногидратом. Другое объяснение этого явления приводится в разд. [20]
В то же время в таких солях, как ( Соеп2Вг2) Вг-НВг-2Н2О и ZnCb - / HCl-I - O, с тем же отношением Н: Н201: 2 присутствуют ионы HsO2, аналогичные ионам, найденным в ряде гидратов кислот. [21]
На олиновую кислоту ( высыхающих масл) азотная кислота сильно действует, превращая ее в пробочную кислоту и в смолистую массу С8Н702, которая, хотя трудно разлагается, но при дальнейшем действии переходит, наконец, также в пробочную кислоту: С8Н702 - J - 02 одному атому гидрата пробочной кислоты. [22]
Структуры гидратов кислот и кислых солей особенно интересны тем, что некоторые или все протоны в них могут присоединяться к молекулам воды с образованием НзО или более сложных ионов. Спектры ПМР показывают, что в моногидратах ряда кислот ( HNOs, НС1С4, HoSCb, H2PtCb) существуют группировки, состоящие из трех атомов водорода, расположенных в вершинах равностороннего треугольника. Существование коротких расстояний О - Н - О ( 2 4 - - 2 6 А) между некоторыми парами атомов кислорода, которые связаны с другими атомами кислорода более длинными водородными связями ( 2 7 - н2 8 А), принято считать признаком образования Н5О24, НуОз4 или более сложных ионов гидроксония, хотя такая интерпретация не всегда однозначна. [23]
Когда вода образует более прочную связь с кислотой, чем реагент, то выгодным процессом оказывается экстракция гидрата кислоты. Стабилизация гидрата кислоты в органической фазе осуществляется путем участия протонов воды в водородных связях. [24]
Вода реагирует с Р2О5, как основание. Различие свойств гидратов кислоты, сохраняющееся в течение продолжительного времени и в водном растворе, свидетельствует о том, что присоединившаяся вода прочно входит в состав гидратов. При замещении воды другими основаниями получаются соли, реакции осаждения которых одинаковы с реакциями соответствующих кислот. Поэтому надо думать, что и строение солей и кислот одинаковое. [25]
Их окислы МоО3 и WOa вследствие высокой валентности металла являются ангидридами. Им отвечают в качестве гидратов кислоты: Н2МоО4 - молибденовая и H2WO4 - вольфрамовая. [26]
Тело А не соединяется с В, но получается из АС при действии аа BD ( см. введение), когда происходит CD. Вода не соединяется с кислородом, но в виде гидрата кислот действует на соединение кислорода с окисью бария, ибо эта окись с кислотным ангидридом дает соль. Заметим, что переход окиси бария ВаО в перекись ВаО2 сопровождается выделением 12 100 единиц тепла на 16 вес. Перекись бария, действуя на кислоту, очевидно, разовьет менее тепла, чем окись, и вот эта-то разность тепла скрывается в перекиси водорода. [27]
Триолы являются гидратами карбоновых кислот. Замещение водородных атомов скелета карбоновой кислоты отрицательными заместителями должно, согласно развиваемым нами представлениям, не только упрочивать гидраты кислот, но и повышать их константу диссоциации за счет оттяжки всех валентных электронных пар к этим заместителям, протонизуя тем самым водородный атом карбоксила. Поэтому способность карбоновых кислот образовывать кристаллогидраты должна вызываться и объясняться теми же причинами, что и повышенная константа диссоциации. Следовательно, сравнительно слабые кислоты не могут давать кристаллические гидраты, а сильные кислоты могут. Связь между наличием отрицательных заместителей в частице карбоновой кислоты, их расстоянием от карбоксила и константой диссоциации кислоты замечена давно. С нашей точки зрения эта связь является частным случаем вицинального эффекта. Насколько мне известно, связь между высокой константой диссоциации кислот и способностью их образовывать кристаллогидраты отмечена ранее не была. Факты подтверждают и этот вывод из представления о вицинальном эффекте. [28]
 |
Окружение молекул воды в кристаллах. Большие заштрихованные кружки - М, ОН -, F - или атомы кислорода кислородсодержащих ионов. [29] |
ОН-группы поляризуются до такой степени, что образуются связи О - Н - О; аналогичный эффект наблюдается и в гидратах. В гидратированных оксосолях и гидроксидах короткие расстояния ( 2 7 - - 2 9 А) между атомами кислорода молекул воды и атомами кислорода оксо-ионов похожи на аналогичные расстояния, найденные в структурах некоторых гидроксидов и гидроксид-оксидов, что свидетельствует об образовании водородных связей. Отдельно мы рассмотрим гидраты кислот и кислых солей, в которых протоны связаны с некоторыми ( или всеми) молекулами воды с образованием катиона оксония Н30 или более сложных группировок. [30]
Страницы: 1 2 3