Гидрат - перекись
Cтраница 2
Добавлением перекиси водорода по методике, описанной в работе 11.4, осаждают гидрат перекиси урана, который после промывки и высушивания при температуре 350 - 400 С переводят в трехокись. [16]
Для исследования термической устойчивости UO4 2Н2О снимают на пирометре Курнакова кривую нагревания гидрата перекиси урана на воздухе в пределах температур от 0 до 900 С; на весах непрерывного взвешивания определяют изменение массы в зависимости от температуры нагревания. [17]
Если в растворе присутствует церий, то выпадает оранжевый, иногда коричневато-красный осадок гидрата перекиси церия. [18]
Соединение С04Н2, очевидно, есть не что иное, как система С03 Н20 ( гидрат перекиси карбонила, надугольная кислота), получающаяся при электролизе. Так же как и эта группа, соединение С04Н2 должно немедленно после образования разлагаться на кислород и углекислоту. Таким образом, получается, что если допускать электролитическое восстановление углекислоты, то электролиз и фотолиз углекислоты идут по той же самой схеме. Аналогия между этими двумя явлениями доходит до полного тождества - потому ли, что солнечные лучи действуют так же, как и электричество ( способствуя диссоциации углекислоты на ионы), или потому, что лучистая энергия превращается в электрическую. [19]
При продолжительном электролизе вся соль, введенная в электролит, переходит в осадок в виде гидрата перекиси и, частично, окиси. [20]
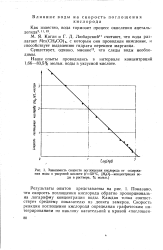 |
Зависимость скорости поглощения кислорода от содержания воды в уксусной кислоте ( 50 С, [ Н2О ] - концентрация воды в растворе, % мольн. [21] |
Мп ( СН3СО) 3, с которым они проводили окисление, и способствует выделению гидрата перекиси марганца. [22]
Соединение Н2СО4 есть, очевидно, не что иное как группа ( С03 Н20) ( гидрат перекиси карбонила), образующаяся при электролизе, которая должна немедленно после своего образования распасться на углекислоту и кислород. [23]
В области температур от - [ - 10 до - 10 С надперекиси натрия и калия взаимодействуют с водяным паром и углекислым газом с выделением только надперекисного кислорода и образованием пероксодикарбо-натов Na и К. Образование последних идет через гидраты перекисей. Термической устойчивостью гидратов перекисей определяется верхний температурный предел образования пероксодикарбонатов при действии углекислого газа на надперекиси. [24]
В присутствии влаги образуются обладающие большой реакционной способностью гидраты перекисей типа НО-R-ООН ( где R - ароматический радикал), которые реагируют с неизмененными молекулами красителя или с волокном или разлагаются с образованием кислот или фенолов. При отщеплении воды от гидратов перекисей светопрочных красителей они могут переходить в более стабильные перекиси. [25]
Она образуется, например, при посыпании раскаленной окиси бария хлоратом калия. После охлаждения и выщелачивания водой хлористого калия получается гидрат перекиси бария. Гидраты перекиси и гидроперекиси мижно путем осторожного рбсзвожинания перевести в чистую безводную перекись. Однако последние следы влаги удаляются с трудом. Так, методом изотермического обезвоживания из октогидрата легко удаляются 7 5 мол. [26]
УСТОЙЧИВОСТЬ перекисей возрастает параллельно усилению электроположительного характера образующих их металлов. Для бериллия перекиси вообще неизвестны; для магния известны только гидраты перекисей; для кальция его безводное. СаОа удается получить лишь обезвоживанием соответствующего октагидрата CaCh-SHaO; перекись стронция SrOa можно получить уже непосредственным действием кислорода на окись стронция, однако лишь при высоком давлении; перекись бария, напротив, легко получается при простом продувании струи воздуха над нагретой окисью бария. ВаОз была известна раньше других перекисных соединений. [27]
Устойчивость перекисей возрастает параллельно усилению электроположительного характера образующих их металлов. Для бериллия перекиси вообще неизвестны; для магния известны только гидраты перекисей; для кальция его безводное перекисное соединение СаОг удается получить лишь обезвоживанием соответствующего октагидрата СаОг - ВНаО; перекись стронция SrOz можно получить уже непосредственным действием кислорода на окись стронция, однако лишь при высоком давлении; перекись бария, напротив, легко получается при простом продувании струи воздуха над нагретой окисью бария. ВаОа была известна раньше других перекисных соединений. [28]
Уран может образовывать перекисные соединения. При действии перекиси водорода на растворы уранилнитрата выпадает желтый осадок гидрата перекиси урана, состав которого отвечает формуле. [29]
Вследствие четырехвалентное кислорода вода должна содержать и ненасыщенные молекулы Н20, ненасыщенность воды нужно считать причиной электролитической диссоциации, - поэтому мыслимо и вполне совместимо с современными взглядами физической химии ( Джонс, Армстронг), что ионы Н и ионы ОН образуют с ненасыщенными молекулами воды неустойчивые соединения. Первый из них представляет не что иное, как гипотетическую недоокись водорода или пергидрид кислорода Н40, металлозамещенное соединение которого Ме40 хорошо известно; второе - представляет собой гидрат перекиси водорода. [30]
Страницы: 1 2 3