Гидратация - катион
Cтраница 1
Гидратация катионов упрочняет комплексный анион. Поэтому существование кристаллогидратов H2SiF6 и отмеченная выше невозможность получения безводной кислоты не противоречат друг другу. Не исключена, однако, возможность то го, чтокрисстал-логидрат H2SiF6 - H2O, в котором содержание воды меньше чем соответствует гидроксониевой соли, на самом деле является кристаллогидратом фтористого кремния. [1]
Гидратация катионов осуществляется по донорно-акцептор-ному механизму, а анионов - за счет водородной связи. [2]
Гидратацию катионов можно рассматривать как образование акво-комплексов, прочность которых определяется величинами констант нестойкости. Легкость, с которой ионы металлов образуют гидраты, возрастает с увеличением их заряда и уменьшением радиуса. Гидраты ионов щелочных металлов нестойки, щелочно-земельных более прочны. Например, гидратированный ион кальция, в основном определяющий жесткость природной воды, может быть представлен в виде октаэдра 1Са ( Н2О) в ] 2, в центре которого находится ион кальция, электростатически связанный с шестью молекулами воды, расположенными в его вершинах. [3]
Гидратацию катионов можно рассматривать как образование акваком-плексов, прочность которых определяется величинами констант нестойкости. Легкость, с которой ионы металлов образуют гидраты, возрастает с увеличением их заряда и уменьшением радиуса. Гидраты ионов щелочных металлов нестойки, щелочноземельных более прочны. [4]
Вследствие гидратации катионов в водных растворах или сольватации в неводных растворах размер диффундирующих молекул может превысить диаметр входных окон. Уменьшение степени ионного обмена может произойти и в том случае, если объем полостей цеолита недостаточен для размещения соответствующего числа обменивающихся катионов. [5]
Числа гидратации катионов, рассчитанные по уравнению (1.60) и данным по у, хорошо согласуются с кристаллографическими радиусами ионов. [6]
Если энтальпия гидратации катиона резко отличается от энтальпии гидратации аниона, то значения ДЯ С 0 и соответствующие соли будут хорошо растворимы в воде. [7]
Первая зона гидратации катиона водорода включает одну молекулу воды. [8]
Вторая зона гидратации катиона водорода при комнатной температуре содержит три молекулы воды. Насколько корректна такая запись. Какие химические связи реализуются в тригидрате катиона оксония. [9]
Уменьшение же степени гидратации катиона разряжающегося металла ( никеля) снижает поляризацию его разряда и увеличивает скорость осаждения. Так, в ряде Li - Na - К и Mg - Са - Sr - Ва радиус ионов возрастает, а степень гидратации уменьшается. Одновременно с этим катодная поляризация при разряде ионов никеля увеличивается. [10]
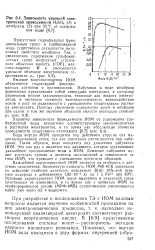 |
Зависимость уДеЛьной электрической проводимости H2SO4 ( I и. [11] |
Явление влагопоглощения ИОМ объясняется гидратацией фиксированных катионов и противоионов. Набухшая в воде мембрана фактически представляет собой твердый электролит, к которому применимы многие закономерности, типичные для жидких электролитов, в частности снижение электростатического взаимодействия ионов и рост их подвижности с уменьшением концентрации раствора электролита. [12]
Во фторидах натрия и лития гидратации катиона, препятствует малый размер аниона фтора. С другой стороны, малые размеры катионов лития и натрия препятствуют присоединению молекул воды анионом фтора за счет водородных связей. [13]
Чтобы объяснить различие в энтальпии гидратации катионов и анионов одинакового размера, Мелвин-Хьюз предположил, что центр молекулы воды не совпадает с центром соответствующего диполя. Картина, основанная на этом предположении, находится в качественном согласии с экспериментальными фактами. [14]
Но если мы постоянно помним о гидратации катионов, допустимо записывать их в очень сокращенной форме. [15]
Страницы: 1 2 3 4