Гидратация - катион
Cтраница 2
 |
Энтропия молекул воды в ближайшем окружении ионов ( а и коэффициент вязкости В в уравнении Джонсона-Дола ( б. [16] |
Отмеченное ион-дипольное взаимодействие наиболее характерно для гидратации катионов, при гидратации анионов со значительным зарядом или малым радиусом более типично присоединение молекул воды за счет водородных связей. [17]
Харман и Пармеле94 показали, что гидратация катионов влияет на величину равновесных значений рН при адсорбции на глинах, а также на теплоты смачивания. Проницаемость, скорость высушивания и прочность в сухом состоянии одноосновных глин тесно связаны со структурой пор, объемом и способностью обмена основаниями. Крупные, о слабые катионы приводят к устойчивой плотной структуре пор, обусловливающей медленное высушивание и высокую прочность в сухом состоянии в сочетании с низкой проницаемостью; наоборот, малые, но сильные ионы, особенно ионы водорода, приводят к обратным эффектам. Отношение теплоты гидратации адсорбированных ионов к теплоте смачивания представляет собой индивидуальную константу, слабо зависящую от природы иона, причем водород представляет исключение. [18]
Величина ДЯ представляет собой сумму теплот гидратации катионов и анионов. Для ее разделения на слагаемые, соответствующие каждому виду ионов, приходится делать более или менее обоснованные допущения. Обычно ( К. П. Мищенко) принимают, что теплоты гидратации ионов цезия и иода равны друг другу. [19]
Показано, что по мере усиления гидратации катионов от натрия к магнию полосы валентных колебаний ОН-групп связанных молекул воды смещаются в низкочастотную сторону, уширяются и сближаются, сливаются в одну в случае перхлората магния. [20]
В принципе аналогичным образом интерпретированы энергии гидратации катионов и анионов. [21]
Полученные результаты показывают, что изотопные эффекты гидратации катионов являются не только количественным отражением большей структурированности тяжелой воды за счет упрочнения водородных связей при замене атомов протия на атомы дейтерия. Они свидетельствуют также о наличии у воды развитой трехмерной структуры, определяющей специфичность свойств воды как растворителя. D в метаноле значительно меньше, чем в воде. Это свидетельствует о качественно иной природе действия ионов на воду по сравнению со спиртами. В частности, делается вывод, что эффекты разрушения присущи только водным растворам. [22]
Гсоли должно обусловливаться не только изменением степени гидратации катиона, но и степени гидратации аниона. [23]
В случае солей любого из анионов понижение энергии гидратации катиона при переходе сверху вниз по группе элементов должна приводить к уменьшению растворимости, тогда как уменьшение энергий решеток должно способствовать увеличению растворимости. Поэтому не удивительно, что для большинства анионов растворимости при переходе от Mg к Ва имеют максимум или минимум. В общем соли, для которых наблюдается максимум ( что указывает на более сильную зависимость энергии решетки от радиуса катиона, чем для энергии гидратации), более растворимы ( доминирующую роль играет энергия гидратации), а соли, для которых наблюдается минимум ( энергия решетки меньше зависит от радиуса катиона, чем энергия гидратации), менее растворимы. [24]
Определение точных значений этих радиусов должно облегчить понимание сравнительной гидратации катионов и анионов и области специфической Ориентации воды вокруг ионов. [25]
 |
Разности значений V cr полученных Бэггом и Рехнитцем и Диком.| Числа гидратации катионов в водных растворах 1 1-галогенидов. [26] |
Нетрудно видеть, что новые, исправленные значения чисел гидратации катионов, как и прежние их значения, основанные на работе Стокса и Робинсона ( см. табл. 3.3), зависят от природы аниона. Иначе говоря, числа гидратации электролитов по-прежнему оказываются неаддитивными по составляющим их ионам. Это еще раз указывает на внутреннюю несогласованность концепции Бейтса и Робинсона. [27]
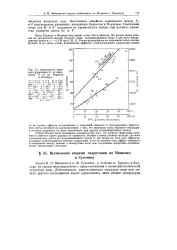 |
Зависимость энергии гидратации Uc от параметра Р ( г по Берналу и Фаулеру. [28] |
Работа Фервея была посвящена доказательству того, что энергия гидратации катионов и анионов одного радиуса не одинакова. Он также не учел всех эффектов, которыми сопровождаются явления гидратации, хотя он впервые учел эффект взаимного отталкивания между ионами и молекулами воды при гидратации вследствие проникновения электронных оболочек. [29]
Содержание воды в частице размером меньше микрона зависит от состояния гидратации катиона: сильно гидратированные ионы, такие, как натрий, снижают обогащение водой внутри частицы, а также способность набухания. Если натриевая глина выщелачивается, молекулы воды входит в частицы и заставляют их набухать. Одновременно эффективный гидролиз благоприятствует диспергированию системы. Поэтому частицы размером меньше микрона с гидратированными ионами, например натриевых или литиевых глин, в чистой воде иловато-вязкие: их свойства приближаются к свойствам гидрофильного золя. [30]
Страницы: 1 2 3 4