Гидратация - белок
Cтраница 1
Гидратация белка также находится в определенной зависимости от рН раствора: она наименьшая в изоточке. Вполне понятно, что с изменением формы белковых молекул и степени их гидратации связано изменение целого ряда свойств белков и их растворов. Так, например, вязкость растворов имеет минимум в изоточке, поскольку свернутые в плотные клубки молекулы оказывают меньшее сопротивление потоку жидкости, чем длинные цепеобразные молекулы. [1]
Для гидратации белка наибольшее значение имеют пептидные связи, за счет которых притягивается примерно 2 / з всей гидратационной воды. В общем частицы гидрофильных коллоидов связывают значительные количества в от. [2]
Для гидратации белка наибольшее значение имеют пептидные связи, за счет которых притягивается примерно 2 / 3 всей гидрата-ционной воды. В общем частицы гидрофильных коллоидов связывают значительные количества воды: так, 1 г сухого крахмала при растворении связывает 0 18 г воды, 1 г яичного альбумина ( белка) - 0 35 г воды, 1 г карбоксигемоглобина - 0 353 г воды. В свою очередь, гидра-тированное вещество также приобретает иные свойства: повышается его устойчивость в растворе, уменьшается скорость диффузии и др. Вязкость и скорость образования внутренних структур в этих растворах значительно выше, чем в коллоидных. [3]
Для гидратации белка наибольшее значение имеют пептидные связи, за счет которых притягивается примерно 2 / з всей гидрата-ционной воды. В общем частицы гидрофильных коллоидов связывают значительные количества воды: так, 1 г сухого крахмала при растворении связывает 0 18 г воды, 1 г яичного альбумина ( белка) - 0 35 г воды, 1 г карбоксигемоглобина - 0 353 г воды. В свою очередь гидратировашюе вещество также приобретает иные свойства: повышается его устойчивость в растворе, уменьшается скорость диффузии и др. Вязкость и скорость образования внутренних структур в этих растворах значительно выше, чем в коллоидных. [4]
Попытки исследовать гидратацию растворенных белков были предприняты еще до того, как было изучено поведение при гидратации сухих белков. При этих исследованиях предполагалось, что часть воды в белковых растворах находится в свободном состоянии, остальная же часть - присоединена к белку. Для определения количества свободной и связанной с белком воды применяются различные методы. Один из них основан на измерении увеличения объема, которое наблюдается при замерзании раствора. Поскольку плотность льда значительно ниже, чем плотность воды, замерзание свободной воды сопровождается отчетливым увеличением объема, которое может быть измерено при помощи дилатометра. Было высказано предположение, что именно эта часть воды и представляет собой гидратную воду. [5]
Одновременно изменяется и гидратация белка, она наименьшая в изоточке. С изменением формы и гидратации белка связано изменение ряда свойств белков и их растворов. Так вязкость растворов имеет минимум в изоточке, так как плотные клубки оказывают меньшее сопротивление потоку жидкости, чем молекулы в развернутом состоянии. Другие свойства, как растворимость, осмотическое давление, светорассеяние, также имеют минимум или максимум в изоточке. Поэтому определение изо-точки белка возможно как прямыми, так и косвенными методами. [6]
Таким образом, определение степени гидратации белков является очень трудной задачей. Поэтому для ряда конкретных целей более целесообразно рассматривать величину, которая может быть точно выражена. Такой величиной является парциальный удельный объем белка и. Эта величина показывает увеличение объема, которое происходит при добавлении 1 г белка к очень большому объему растворителя. [7]
Эта электропроводность существенно зависит от степени гидратации белка. Можно думать, что она определяется примесями, в частности ионными, и не имеет биологического значения. [8]
Нет сомнения в том, что концепция гидратация белка важна и даже полезна, особенно если не делается попыток определить это понятие слишком буквально. Вода во всех своих состояниях взаимодействует с белком, образуя на поверхности белковой молекулы идентифицируемый слой. Так, водяной пар конденсируется на поверхности высушенных порошкообразных белков; при этом первый слой ( монослой) связывается очень прочно. [9]
Суммируя вышеизложенное, можно заключить, что исследование гидратации сухих белков позволяет нам изучить динамику процесса и определить количество прочно связанной воды. Однако последнее слишком мало, чтобы образовать монослой ориентированных молекул воды на поверхности макромолекулы белка. Изучение же дальнейшего процесса связывания воды не позволяет нам достаточно четко определить те количества ее, которые идут на дополнение этого монослоя и на образование вторичного слоя ориентированных диполей воды. Таким образом, этот метод не дает возможности определить количество гидратнои воды в расчете на молекулу белка, не говоря уже о толщине гидратнои оболочки его молекулы. [10]
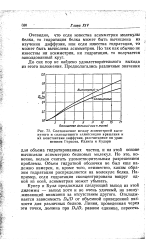 |
Соотношение между асимметрией вытянутого и сплющенного эллипсоидов вращения и их константами диффузии, рассчитанное по уравнениям Герцога, Иллига и Кудара. [11] |
Очевидно, что если известна асимметрия молекулы белка, то гидратация белка может быть вычислена из изучения диффузии, или если известна гидратация, то может быть вычислена асимметрия. Но так как обычно не известны ни асимметрия, ни гидратация, то получается заколдованный круг. [12]
Пользуясь этим свойством связанной воды, Соренсен разработал способ определения гидратации белков. Гортнер и Ньютон определяли количество связанной воды, используя метод криоскопии. Думанский предложил очень удачный рефрактометрический и поляриметрический методы определения. [13]
Литературные данные и результаты экспериментов, обсуждаемые ниже, описывают процесс гидратации белка, при котором вода добавляется к белку до получения раствора. Представление о процессе гидратации белка, который однозначно описывается на основании такого эксперимента, следует различать от концепции гидратационной воды, рассмотренной с различных точек зрения в соответствии с интересами исследователей и характером использованных экспериментальных методов. [14]
В химии белка мы часто встречаемся с необходимостью определить либо степень гидратации сухих белков в атмосфере водяного пара, либо степень гидратации белков, растворенных в больших количествах воды. [15]
Страницы: 1 2 3 4