Гидратация - белок
Cтраница 3
Ближе отвечает действительности представление, согласно которому [10] осмотическое давление определяется разницей в активности молекул воды по обе стороны мембраны. В то время как вода, в которую погружен осмометр, обладает полной активностью свободной воды, активность воды с внутренней стороны мембраны снижена гидратацией белка, а также иммо-билизирующим действием нитевидных белковых молекул. [31]
Под гидратацией понимают взаимодействие молекул воды с молекулами сухого или растворенного вещества. В живом организме веществами, связывающими воду, являются главным образом белки, а так как вода является универсальной средой для биологических реакций, то большое значение гидратации белков не требует особых доказательств. Литература по этому вопросу содержит много противоречивых данных. Это объясняется тем, что гидратация сухих и растворенных белков исследовалась многими авторами и притом различными методами. Так, например, одни авторы изучали гидратацию сухого белка, понимая под ним воздушносухой препарат, другие же при исследовании этого процесса использовали действительно сухие, не содержащие воды препараты. Хорошо известно, что сухие белки связывают воду, даже находясь на воздухе нормальной влажности, и если не учитывать этого обстоятельства, то можно допустить серьезные ошибки. [32]
 |
Строение цепей главных валентностей целлюлозы ( а и крахмала ( б ( атомы кислорода заштрихованы. [33] |
Гидратация и сольватация белков приводит к изменению структуры и свойств белковой молекулы, что имеет большое значение в различных процессах взаимодействия белков с веществами среды. Сорбированные молекулы неэлектролитов вклиниваются между витками полипептидной цепи и разрывают водородные связи между ними. Гидратация белков влияет на вязкость их растворов. [34]
Гидратация и сольватация белков приводят к изменению структуры и свойств белковой молекулы, что имеет большое значение в различных процессах взаимодействия белков с веществами среды. Сорбированные молекулы неэлектролитов вклиниваются между витками полипептидной цепи и разрывают водородные связи между ними. Гидратация белков влияет на вязкость их растворов. [35]
 |
Схематическое изображение сигнала ЯМР, зарегистрированного в дифференциальной форме. [36] |
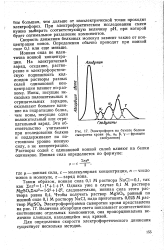
Обнаружено четыре типа структуры воды: жидкая, капиллярная, сильносвязанная и слабосвязанная. Файнер наблюдал специфическое расщепление сигналов, которое является характеристичным для каждого типа гидратной оболочки, и отметил, что данные о релаксации позволяют судить об ориентации и анизотропном характере движения молекул воды. Работа Линча и Уэбстера [103] показывает, что ЯМР является эффективным методом изучения гидратации белков, позволяющим исследовать подвижность, неоднородность и анизотропию молекул воды в гидратной оболочке. [37]
 |
Электрофорез на бумаге белков. [38] |
Ионная сила не идентична ионной концентрации. На электрический заряд, оседание, растворение и электрофоретиче-скую подвижность коллоидов растворы разных солей одинаковой концентрации влияют по-разному. Ионы, несущие несколько положительных и отрицательных зарядов, оказывают большее влияние на гидратацию белка, чем ионы, несущие один положительный или отрицательный заряд. [39]
Если обратиться к литературным данным, то мы встречаемся с некоторыми данными, указывающими на то, что соли могут оказывать влияние на положение изоэлектрической точки. Так, Паули в своей работе относительно Ионизации, гидратации и оптического вращения белковых веществ [3] говорит: Нейтральные соли понижают ионизацию белковых веществ вследствие образования нейтральных комплексов. Характерным здесь является то, что при электроотрицательном белке соли щелочноземельных металлов понижают ионизацию и гидратацию белка значительно сильнее, чем соли щелочных металлов. На основании этого можно предполагать, что образующаяся при титровании соль ( NaCl) будет уменьшать ионизацию желатины, а это в свою очередь должно будет сказаться в понижении изоэлектрической точки. [40]
Так, например, известно, что в покоящейся мышце большая часть ионов калия находится в связанной форме и неспособна диализироваться; однако сразу же после сокращения мышцы эти ионы легко переходят в диализат. Ионы калия, вероятно, отщепляются от отрицательно заряженных карбоксильных групп миозина и других мышечных белков. Это уменьшение объема мышцы можно объяснить тем, что количество свободной воды в ней уменьшается в связи с гидролизом или гидратацией белков или других ионов. [41]
Белковые вещества обладают способностью связывать значительные количества воды - гидратироваться. Важность гидратации белков видна из того, что вода представляет собой универсальную среду биологических реакций. Гидратация состоит в связывании дипольных молекул воды с ионами или ионными группами, а также с диполями или полярными группами; она происходит и в растворах, и в твердых веществах. Значительную гидратацию белков обусловливает наличие на поверхности их молекул большого количества разнообразных полярных, в том числе ионогенных, групп. Количество гидратационной воды, связанной с альбуминами и глобулинами, составляет 0 2 - 0 6 г на 1 г сухого веса белка. [42]
Под гидратацией понимают взаимодействие молекул воды с молекулами сухого или растворенного вещества. В живом организме веществами, связывающими воду, являются главным образом белки, а так как вода является универсальной средой для биологических реакций, то большое значение гидратации белков не требует особых доказательств. Литература по этому вопросу содержит много противоречивых данных. Это объясняется тем, что гидратация сухих и растворенных белков исследовалась многими авторами и притом различными методами. Так, например, одни авторы изучали гидратацию сухого белка, понимая под ним воздушносухой препарат, другие же при исследовании этого процесса использовали действительно сухие, не содержащие воды препараты. Хорошо известно, что сухие белки связывают воду, даже находясь на воздухе нормальной влажности, и если не учитывать этого обстоятельства, то можно допустить серьезные ошибки. [43]
Если результаты гидродинамических измерений интерпретировать упрощенно, то можно прийти к выводу, что гидратацион-ные слои дают вклад в инерционность молекулы белка ( в растворе), а время жизни молекулы воды в этих слоях должно быть велико но сравнению с характеристическим временем движения белковых молекул. Например, если ориентационные времена релаксации больших белковых молекул, согласно, скажем, измерениям частотной зависимости диэлектрической проницаемости или вычислениям из закона Стокса, составляют 10 - 5 с, то можно ожидать, что продолжительность их жизни будет значительно больше. Однако такая точка зрения неправильна. Чтобы объяснить данные гидродинамических измерений, достаточно предположить, что при гидратации белка молекула воды находится в определенном положении. Если это условие удовлетворяется ( а для этого молекула воды должна резко изменить свой угловой момент инерции, как если бы она внедрялась в массу растворителя или же покидала его), то продолжительность жизни молекулы воды может быть меньше, чем время, которое характеризует движение белка и еще дает вклад в инерционность белковых молекул. На то, что это требование удовлетворяется, указывают рентгенографические данные, согласно которым многие молекулы воды в гидратационном слое находятся в определенных положениях. [44]
Основными гидрофильными коллоидами ткани являются белки, и нельзя сильно изменять природу тканевых белков и в то же время поддерживать жизнь. В ткани, однако, не существует изолированных белковых систем. Вместе с белками и многими другими компонентами в ткани имеются электролиты. Электролиты заставляют белки набухать или сжиматься, в зависимости от осмотических соотношений. Гидратация белков должна рассматриваться как часть общей картины гидратации тканей. Хилл и др. интересовались величиной ошибок, которые могут возникать в физиологических расчетах, не учитывающих присутствия связанной воды. Если белок связывает около 0 35 г воды на 1 г сухого белка, то всего будет связано около 4 5 % общего веса воды. Имеется немного физиологических расчетов, достаточно точных для того, чтобы серьезно считаться с подобной ошибкой. В качестве последнего замечания можно сказать, что хотя еще не ясно, что может дать понятие связанной воды для понимания вопросов физиологии и патологии, но ее значение для понимания природы стабильности белков чрезвычайно велико. [45]
Страницы: 1 2 3 4