Гидратация - электролит
Cтраница 1
Гидратация электролитов в растворах является главной причиной их диссоциации на ионы - она обусловливает устойчивость ионов в растворах и затрудняет ассоциацию ионов. В газовой фазе диссоциация электролитов на ионы - процесс сильно эндотермичный и не происходит самопроизвольно. В разбавленных растворах энергия, выделяющаяся при взаимодействии ионов с водой, в значительной степени компенсирует энергию диссоциации. [1]
Гидратация электролитов в растворе является необходимым условием диссоциации их на ионы - она обусловливает устойчивость ионов и препятствует их ассоциации. Диссоциация электролитов в газовой фазе требует огромной затраты энергии и не протекает самопроизвольно. В растворах же энергия, выделяющаяся при взаимодействии ионов с водой, в значительной степени компенсирует энергию, необходимую для диссоциации. [2]
Природа гидратации электролитов выяснена лишь в общихчертах. [3]
Энергия гидратации электролита равна разности между энергией, необходимой для превращения моля кристаллического электролита в ионы, и теплотой растворения. Теплота растворения легко измеряется с помощью стандартной калориметрической техники, но энергию испарения кристаллической соли получить труднее. Энергия испафения известна как энергия решетки, и она вычисляется с помощью сложного цикла Борна - Габера, который здесь рассматриваться не будет. [4]
Природа гидратации электролитов выяснена лишь в общих чертах. [5]
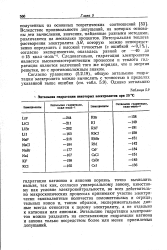 |
Энтальпия гидратации некоторых электролитов при 25 С. [6] |
Следовательно, гидратация электролитов является высокоэкзотерм ическим процессом и теплота гидратации является величиной того же порядка, что и энергия решетки, но с противоположным знаком. [7]
 |
Числа гидратации л для КС1, рассчитанные. [8] |
Найденные экстракционным способом числа гидратации электролитов не выходят за пределы значений, вычисленных другими методами. [9]
Латимером Стоке делит суммарную энергию гидратации электролитов на две части - электростатическую / Gesl и неэлектростатическую AGfs ( электростатическая составляющая разности электростатических, химического потенциала в растворе и в газе) и усредненную величину диэлектрической проницаемости среды в к иону слое. [10]
 |
Числа гидратации электролитов по данным Стокса и Робинсона, Глюкауфа, Бейтса и Робинсона. [11] |
Естественно, что изменение числа гидратации электролита влечет за собой и изменение чисел гидратации составляющих этот электролит ионов. [12]
В литературе имеется мало сведений о сольватации и гидратации электролитов в гидрофобных полимерах. [13]
Следует также отметить известную произвольность выбора значений чисел гидратации электролитов и тем более ионов определенного вида. [14]
Несмотря на то, что Уэбб несколько глубже выяснил сущность гидратации электролитов, чем его предшественники, и получил более точные энергетические величины, некоторые стороны проблемы все же остались недостаточно уточненными. [15]
Страницы: 1 2 3