Гидратация - электролит
Cтраница 3
В этом случае применяется метод, основанный на уравнении Робинсонами Стокса для коэффициента активности с учетом гидратации электролита. [31]
Дебаю - Хюккелю; / - ионная сила раствора; А, В, а - постоянные; h - число гидратации электролита; аю - активность воды; т - моляльность раствора. [32]
 |
Сорбция растворов кислот в пленках полимеров. [33] |
В силу особенностей условий диффузии и протекания реакций в полимерной матрице при исследовании хемостоикости полимеров одним из узловых вопросов является выяснение состояния агрессивной среды в твердом полимере. Знание степени диссоциации и гидратации электролита в полимере необходимо для строгих кинетических расчетов реакций, происходящих в полимере, а также для прогнозирования защитных свойств полимерных покрытий. [34]
То же справедливо и для разности энтальпии гидратации электролитов, содержащих один и тот же катион я разные анионы ( например. Это обусловлено тем, что энтальпия гидратации электролита при достаточно большом разбавлении является аддитивной функцией энтальпии гидратации обоих видов ионов. Таким образом, если экспериментально или теоретически определить энтальпию гидратации хотя бы одного иона, то энтальпию гидратации других ионов можно с успехом вычислить из энтальпии гидратации соответствующих электролитов. Так как это невозможно осуществить даже приближенно, приходится довольствоваться как относительно наиболее пригодным методом получения распределения, основывающимся на 1: 1-электролите, относительно которого делается предположение, что энтальпии гидратации его катиона и аниона одинаковы. [35]
Наряду с данными, полученными по описанным ранее методам, в них включены также результаты расчетов другими методами. В методе Фаянса используются циклы, связанные с применением водородного и амальгамно-калиевого электродов и рассчитываются соответственно теплоты гидратации протона и иона калия. Комбинация полученных таким образом величин с экспериментальными теплотами гидратации электролитов позволяет найти теплоты гидратации любых других ионов. Хотя при этом используется так называемая абсолютная шкала потенциалов Оствальда, которую нельзя считать научно - обоснованной, цифры, полученные Фаянсом, интересны как первые результаты теоретического расчета теплот гидратации. [36]
Однако нельзя однозначно установить, реально ли отражает теория Робинсона и Стокса взаимодействие между ионами и молекулами растворителя. Главная трудность в этом отношении заключается в определении числа молекул воды h, связанных одним молем растворенного вещества, так как методы, предложенные для определения числа гидратации, предельно неопределенны и различные методы приводят к сильно различающимся результатам. Робинсон и Стоке [25] пытались сделать некоторые выводы о числе гидратации электролитов путем сравнения термодинамических условий в растворах электролитов и неэлектролитов. Таким способом ими было вычислено число гидратации некоторых электролитов. Однако их результаты остаются под вопросом и не всегда логичны. Таким образом, для объяснения действительного положения требуются дальнейшие исследования. Одна такая попытка была предпринята Глюкауфом [28], где вместо предыдущих расчетов на основе статистики, использующей мольные доли, была применена статистика на основе объемных долей. Однако эти результаты нельзя считать полностью убедительными, хотя числа гидратации, полученные в этой теории, аддитивны. [37]
 |
Химические коэффициенты активности ионов Са2 и СГ в водных растворах хлорида кальция при 25 С. [38] |
Можно с уверенностью утверждать, что небольшие по размерам двухзарядные ионы Mg2 и Са2 оказывают гораздо более сильное воздействие на окружающую их воду, чем сравнительно крупный однозарядный хлорид-ион. Эти различия выразятся не только в существенном изменении диэлектрической проницаемости воды вблизи катионов Mg2 и Са2, что уже само по себе ставит под сомнение возможность применения расчетных формул метода Бейтса - Робинсона ( см. разд. Кроме того, в случае таких сильно гидратирующихся ионов, как Mg2 и Са2, постулат теории Стокса - Робинсона о постоянстве числа гидратации электролита, вероятно, нарушается уже при сравнительно умеренных концентрациях соответствующей соли. [39]
То же справедливо и для разности энтальпии гидратации электролитов, содержащих один и тот же катион я разные анионы ( например. Это обусловлено тем, что энтальпия гидратации электролита при достаточно большом разбавлении является аддитивной функцией энтальпии гидратации обоих видов ионов. Таким образом, если экспериментально или теоретически определить энтальпию гидратации хотя бы одного иона, то энтальпию гидратации других ионов можно с успехом вычислить из энтальпии гидратации соответствующих электролитов. Так как это невозможно осуществить даже приближенно, приходится довольствоваться как относительно наиболее пригодным методом получения распределения, основывающимся на 1: 1-электролите, относительно которого делается предположение, что энтальпии гидратации его катиона и аниона одинаковы. [40]
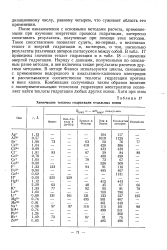 |
Химические теплоты гидратации отдельных ионов. [41] |
После ознакомления с основными методами расчета, применяемыми при изучении энергетики процесса гидратации, интересно сопоставить результаты, полученные при помощи этих методов. Такое сопоставление позволяет судить, во-первых, о величинах теплот и энергий гидратации и, во-вторых, о том, насколько результаты различных авторов согласуются между собой. В табл. 17 приведены значения теплот гидратации и в табл. 18 - значения энергий гидратации. Наряду с данными, полученными по описанным ранее методам, в нее включены также результаты расчетов другими методами. В методе Фаянса используются циклы, связанные с применением водородного и амальгамно-калиевого электродов и рассчитываются соответственно теплоты гидратации протона и иона калия. Комбинация полученных таким образом величин с экспериментальными теплотами гидратации электролитов позволяет найти теплоты гидратации любых других ионов. [42]
Страницы: 1 2 3