Первичная гидратация
Cтраница 3
В макроскопических явлениях, вызванных влиянием растворенных ионов в воде, изменения структуры водных слоев, не контактирующих непосредственно с ионами, наряду с первичной гидратацией также играют роль в явлениях гидратации. Этот эффект, называемый вторичной гидратацией, представляет собой явление, еще более сложное, чем первичная гидратация, с которой он тесно переплетается. Изменение структуры воды обусловлено не только влиянием электрического поля ионов, поскольку ряд экспериментальных фактов указывает на то, что незаряженные молекулы также влияют на структуру жидкости вокруг себя ( см. разд. В этой книге рассмотрены только отдельные аспекты вторичной гидратации. [31]
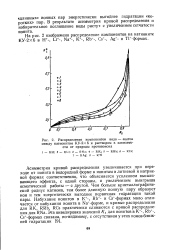 |
Распределение компонентов вода - ацетон между катионитом КУ-2Х6 и раствором в зависимости от природы противоиона. [32] |
Асимметрия кривой распределения увеличивается при переходе от ионита в водородной форме к ионитам в литиевой и натриевой формах соответственно, что объясняется усилением высаливающего эффекта, с одной стороны, и увеличением выигрыша осмотической работы - с другой. Чем больше кристаллографический радиус катиона, тем более длинную ионную пару образует ион и тем энергетически выгоднее первичная гидратация такой пары. [33]
Самойлова получили дальнейшее развитие в работе [179], авторы которой рассчитали потенциальные барьеры, управляющие молекулярным обменом в гидратных оболочках ионов. Основываясь на двухструктурной модели гидратной оболочки, В. М. Вдо-венко и др. [179] нашли, что у каждого иона за слоем первичной гидратации, где молекулы воды прочно связаны с ионом, существует область разрушенной структуры, где потенциальные барьеры, разделяющие соседние положения равновесия, ниже, чем в чистой воде. Приближенная количественная характеристика потенциальных барьеров, полученная ими, в общем согласуется с наблюдаемыми экспериментально свойствами водных растворов электролитов. [34]
Как уже было указано, однократная гидратация углеводородов С13Н22 дает крайне скромные выходы в расчете на 4-пропилизоборнеол, примерно25 - 30 %, считая на углеводород, вошедший в реакцию. В целях увеличения запасов этого алкоголя мы подвергли углеводород, уже бывший в реакции Бортрама-Вальбау - ма, повторной гидратации и убедились в том, что реакция эта прошла вновь и притом с выходами не меньшими, чем при первичной гидратации. [35]
Явление гидратации ( в общем случае, сольватации) заключается в том, что ионы растворенного вещества окружены растворителем и движутся с некоторой его частью, вступающей с ним во взаимодействие. Различают первичную ( ближнюю) и вторичную ( дальнюю) гидратации. Первичная гидратация заключается в прочном связывании ионов молекул воды, вплоть до образования донорно-акцепторных связей. Вторичная - представляет собой электростатическое взаимодействие молекул воды с первично гидратированными ионами. Энергетический эффект гидратации довольно значителен и составляет примерно 300 - 4000 кДж / моль. [36]
Явление гидратации ( в общем случае, сольватации) заключается в том, что ионы растворенного вещества окружены растворителем и движутся с некоторой его частью, вступающей с ним во взаимодействие. Различают первичную ( ближнюю) и вторичную ( дальнюю) гидратации. Первичная гидратация заключается в прочном связывании ионом молекул воды, вплоть до образования донорно-акцеп-торных связей. [37]
Большой размер и относительно слабое взаимодействие анионов МХ4 с водой сами по себе недостаточны, чтобы обеспечить хорошую экстракцию. Необходимо при этом принимать во внимание и катион-партнер. С другой стороны, небольшие или многозарядные катионы с заметной первичной гидратацией нелегко переходят в органическую фазу и экстракция таких катионов может быть слабой. Однако особые свойства водородного иона ( см. § 5), которые определяют его необычно сильную сольватацию основными органическими молекулами, обеспечивают очень хорошую экстракцию комплексных анионов основными органическими растворителями. [38]
Измерения поглощения в области 1 мкм оыли приведено. По данным этих авторов, ионы окружены двумя гидратными сферами: в сфере первичной гидратации молекулы воды прочно удерживаются ионом вследствие электростатического ион-дипольного притяжения; в сфере вторичной гидратации молекулы воды относительно слабо связаны с молекулами воды из сферы первичной гидратации и со свободными молекулами воды водного окружения. [39]
Молекулы гидратной воды, адсорбированные на ионах, постоянно обмениваются с молекулами в объеме жидкости ( см. разд. Можно предположить, что обмен требует растяжения связи между ионом и адсорбированной на нем молекулой воды примерно на 0 8 А. Отношение энергии Ah, требуемой для растяжения этой связи, и энергии Aw влияет на первичную гидратацию. Если A / iiAiw, то молекула воды, адсорбированная на ионе, образует более сильную связь с ионом, чем с соседней молекулой воды; это явление, согласно Самойлову, можно назвать положительной гидратацией. При таких условиях соседние молекулы воды проводят в среднем больше времени у иона, чем в состоянии связи между собой. [40]
Рассмотрим качественно влияние увеличения концентрации электролита на ( CPl - CPl), опираясь на представления, развитые нами в предыдущих главах. Так как добавление 1 моль к бесконечно большому количеству раствора не ведет к изменению концентрации, то не должны изменяться и межионные расстояния. До ГПГ пока вода имеется в избытке, при этих же условиях не должна меняться и первичная гидратация ионов. [41]
Измерения поглощения в области 1 мкм оыли приведено. По данным этих авторов, ионы окружены двумя гидратными сферами: в сфере первичной гидратации молекулы воды прочно удерживаются ионом вследствие электростатического ион-дипольного притяжения; в сфере вторичной гидратации молекулы воды относительно слабо связаны с молекулами воды из сферы первичной гидратации и со свободными молекулами воды водного окружения. [42]
Для правильного учета взаимодействий между ионами и молекулами воды важным моментом является сила связи между ионом и молекулами воды по сравнению с силой связи между самими молекулами воды. Более того, определяющим фактором в этом отношении является не энергия, требуемая для разрыва связей между соседними молекулами воды ( что требуется для испарения), а энергия ( Дау), необходимая для растяжения связи между соседними молекулами воды на сравнительно короткое расстояние Аг, достаточное для того, чтобы произошел обмен данной молекулы воды с другой молекулой. Это расстояние Аг в водных растворах примерно равно 0 8 А; энергия Aw, требуемая для такого растяжения, связана с ближней ( первичной) гидратацией. Таким образом, первичную гидратацию действительно можно рассматривать как адсорбцию молекул воды на ионах. [43]
Экспериментальные числа гидратации очень сильно зависят от того, какие свойства раствора исследуются. Методы, перечисленные в группе а табл. 6, вероятно, дают число первичной гидратации; метод по-движностей, который также может использоваться для оценки первичной координации растворителя [53], как уже отмечалось выше, в данном случае неприменим. Методы группы б учитывают суммарные эффекты, вызванные как первичной, так и вторичной гидратацией и включающие молекулы воды, на которые поле иона оказывает косвенное влияние. В группе в представлены методы, дающие обычно [95, 53] число первичной гидратации, но приводящие к неожиданно низким значениям для протона. [44]
Обращает на себя внимание разница в переносе ЕР-ионов через катио-нообменную мембрану и ОН - - ионов через анионообменную. В силу каких-то причин перенос Н - ионов практически совсем подавлен. Кук [9] видит в этом проявление взаимодействия противоиона и растворителя. Первичная гидратация катионов вызывает нарушение нормального пространственного расположения диполей воды, В результате они становятся сравнительно неактивными, и диссоциация воды в околомембранном слое, через который движутся катионы, оказывается подавленной. Этот эффект гораздо слабее выражен у анионов. Поэтому около анионообменной мембраны находится слой нормально ионизированной воды. Данное объяснение не кажется вполне убедительным. Очевидно, вопрос о различном поведении катионо - и анионообменных мембран заслуживает дополнительного изучения. [45]
Страницы: 1 2 3 4