Дальняя гидратация
Cтраница 1
Дальняя гидратация всегда сопровождается выделением довольно больших количеств энергии при переходе ионов в раствор. [1]
Различают ближнюю и дальнюю гидратацию. Первая характеризует взаимодействие ионов с ближайшими молекулами воды. [2]
Вопрос о ближней и дальней гидратации ионов Крестов рассматривает с позиций преимущественного взаимодействия ион - молекулы воды и влияния возникающего комплекса на связи между самими молекулами воды. При оценке первого взаимодействия, названного термодинамической гидратацией, решающее значение имеет первичная гидратация ионов, определяющая структуру образующихся гидратов и вносящая наибольший вклад в энергетику процесса. Кроме координационных чисел, которые в данном случае имеют целочисленное значение, важнейшими количественными характеристиками процесса гидратации являются изменения термодинамических величин - энтальпии, энтропии, теплоемкости и изобарно-изотермического потенциала. [3]
Самойлов ввел термины ближняя и дальняя гидратация, смысл которых близок к терминам первичная и вторим пая сольватация. [4]
Для нарушения структуры гидратной оболочки в области дальней гидратации необходимо, чтобы магнито-гидродинамическое давление жидкости превышало предельное напряжение сдвига то. [5]
Статья [3208], в которой рассматриваются энтропийные характеристики ближней и дальней гидратации, типична для первой группы; для второй типичны статьи [3216, 3218], в которых используют линейную взаимосвязь между энтропией растворения и теплотой гидратации. В качестве примера из третьей группы можно привести работу [3227], в которой найдена зависимость между энтропией ионов в растворе и их подвижностью. [6]
Опыты показывают, что при электромагнитном воздействии на растворы дальняя гидратация ионов и их ассоциатов претерпевает изменения. [7]
Статья [ 32081, в которой рассматриваются энтропийные характеристики ближней и дальней гидратации, типична для первой группы; для второй типичны статьи [3216, 3218], в которых, используют линейную взаимосвязь между энтропией растворения и теплотой гидратации. В качестве примера из третьей, группы можно привести работу [3227], в которой найдена зависимость между энтропией ионов в растворе и их подвижностью. [8]
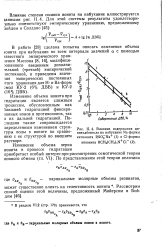 |
Влияние содержания ди-винилбензола на набухание Na-формы катионита RSO - Na ( 1 и Cl-формы. [9] |
Изменение объема ионита при гидратации является сложным нроцессом, обусловленным как ближней гидратацией фиксированных ионов и противоионов, так и их дальней гидратацией. [10]
 |
Относительное изменение скорости ультразвука в водных растворах солей. [11] |
На абсолютное значение Л5дальн наиболее существенное влияние оказывает заряд ионов и меньше - их размер, соответственно изменяются и числа молекул воды в области дальней гидратации. [12]
Рассматриваемые в настоящем сообщении величины ASn ( AS n) характеризуют суммарное изменение энтропии воды как в области ближней, так и в области дальней гидратации иона. [13]
Кроме ближней гидратации, с которой главным образом связаны так называемые кинетические свойства растворов и механизм протекания в них ряда процессов, в том числе растворения, существует еще так называемая дальняя гидратация, связанная с взаимодействием с более удаленными объемами воды. Дальняя гидратация свойственна в основном заряженным частицам - ионам, она состоит главным образом в поляризации под действием поля иона окружающих объемов воды и при переходе иона в раствор сопровождается всегда выделением довольно больших количеств энергии. Структура разбавленных водных растворов соответствует наименьшему возможному изменению структуры воды при образовании раствора. [14]
Первое слагаемое - отрицательный вклад в 2ДУ ГИдр, суммарно характеризующий процессы перехода ионов из газовой фазы в раствор, взаимодействия ион-молекула воды ( положительные вклады, связанные с эффектами отталкивания [79], невелики и могут не учитываться) и упорядочивания расположения молекул в поле ионов в области дальней гидратации. Второе слагаемое - положительный вклад, суммарно характеризующий эффект разрушения структуры воды, связанный с разрывом водородных связей между молекулами воды и их переориентацией в поле иона. [15]
Страницы: 1 2 3