Дальняя гидратация
Cтраница 2
При этом взаимодействие воды с глинистой породой характеризуется с позиций молекулярно-кинетической теории гидратации ионов О.Я. Самойлова, заключающейся в том, что гидратация ионов в водных растворах рассматривается не как связывание какого-либо числа молекул воды ионами, а как влияние последних на трансляционное движение ближайших молекул воды и поляризацию более удаленных - ближняя и дальняя гидратация ионов. [16]
Кроме ближней гидратации, с которой главным образом связаны так называемые кинетические свойства растворов и механизм протекания в них ряда процессов, в том числе растворения, существует еще так называемая дальняя гидратация, связанная с взаимодействием с более удаленными объемами воды. Дальняя гидратация свойственна в основном заряженным частицам - ионам, она состоит главным образом в поляризации под действием поля иона окружающих объемов воды и при переходе иона в раствор сопровождается всегда выделением довольно больших количеств энергии. Структура разбавленных водных растворов соответствует наименьшему возможному изменению структуры воды при образовании раствора. [17]
Ближняя гидратация заключается в прочном удерживании ионом определенного числа молекул воды, которые передвигаются вместе; ионом. Дальняя гидратация охватывает взаимодействие иона с молекулами воды за пределами первой гидратной оболочки и заключается главным образом в поляризации под действием электрического поля иона окружающих объемов воды. [18]
Нам представляется, что значительную роль могут играть большие ускорения движения ионов в начальный момент вхождения в магнитное поле, особенно высокоградиентное. При таком ускорении дальняя гидратация ионов может на какое-то мгновение уменьшиться, что также способствует взаимодействию противоионов. [19]
Следует отметить, что отрицательные дифференциальные теплоты сорбции калиевой, цезиевой и таллиевой форм ионита наблюдаются только после сорбции первых четырех молей воды, именно тогда, когда создаются предпосылки для проявления эффекта отрицательной гидратации. Последняя может осуществляться лишь под влиянием сформировавшегося порядка дальней гидратации, как следует из современной теории гидратации. [20]
Этот вывод не противоречит отмеченному выше факту увеличения абсолютных величин АН тиар и A5 r Hp при переходе от однозарядных ионов к двух - и трехзарядным. Дело в том, что при увеличении заряда происходит резкое усиление вклада дальней гидратации и общее увеличение упорядочивающего влияния ионов. [21]
Влияние ионов на структуру воды связано с их гидратацией. Различают ближнюю гидратацию ( взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию - поляризацию более отдаленных молекул воды. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. На основании данных о растворимости солей и теплотах гидратации ионов установлено, что на связь одной молекулы с катионом в зависимости от его заряда ( 1, 2 или 3) приходится соответственно 42, 126 или 420 кДж / моль. В последнем случае гидратиро-ванный катион похож на химическое соединение. [22]
Влияние ионов на структуру воды связано с их гидратацией. Различают ближнюю гидратацию ( взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию - поляризацию более отдаленных молекул воды. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. В последнем случае гидратированный катион похож на химическое соединение. [23]
При дальнейшем увеличении влажности молекулы воды начинают связываться менее активными центрами адсорбции - структурными группами ОН и О2 поверхности минералов - ПРИ помощи водородной связи. Одновременно продолжается формирование молекул воды вокруг наиболее активных центров поверхности глинистых минералов в результате их дальней гидратации. При влажности, соответствующей гигроскопичности глин при p / ps 0 5, на поверхности глинистых минералов образуется монослой из молекул воды. [24]
С другой стороны, в электрическом поле ионов повышается упорядочивать молекул BCJUI вне первого слоя и снижается энтропия ( вторичная гидратация по Ьскрису или дальняя гидратация по Самойлову), т.к. воздействия электрического поля распространяется и на области с искаженной структурой С учетом сказанного было предложено вводить карбонатсодер-жащие добавки и в частнссти-тверднй остаток отходов содового про - изводотва. [25]
Указывалось [86], например, что гидратные числа ионов имеют дробные значения, поскольку они отражают в условиях межионного взаимодействия как ближнюю, так и дальнюю гидратацию. [26]
Это явление подтверждено Н. И. Мелиховой и С. Ф. Дудкиным на примере омагни-чивания раствора сульфата железа. Оказалось, что в этом случае снижается отрицательная адсорбция ионов железа на поверхности раздела раствор - воздух. Таким образом, временное изменение магнитной обработкой дальней гидратации ионов в водных системах может явиться одним из существенных механизмов регулирования физико-химических свойств последних. [27]
Первичная гидратация - это те молекулы воды, которые прочно удерживаются ионами и движутся вместе с ними, составляя единое целое. Вторичная гидратация же охватывает взаимодействия ионов с молекулами растворителя вне предела первичной гидратной оболочки. Самойлов [12] предпочел называть эти два вида гидратации ближней и дальней гидратацией. Вторичная, или дальняя, гидратация не зависит от специфических взаимодействий молекул растворителя с ионами растворенного вещества, вследствие чего ее можно удовлетворительно рассмотреть при помощи классических электростатических теорий, например при помощи уравнения Борна, предположив при этом непрерывность растворителя. В соответствии с этими соображениями ограничим термин гидрофильная гидратация пространством вблизи иона, подвергающегося специфическим взаимодействиям. Процессы гидратации, возникающие на далеких расстояниях от этого иона, можно определить как поляризационную гидратацию. [28]
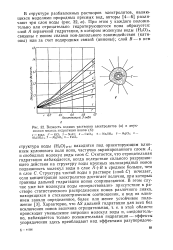 |
Вязкость водных растворов электролитов ( а и двух-зонная модель гидратации ионов ( б. [29] |
Считается, что отрицательная гидратация наблюдается, когда вследствие сильного разрушающего действия на структуру воды крупных малозарядных ионов подвижность молекул воды в слое А - - В в среднем больше, чем в слое С. Структура чистой воды в растворе ( слой С) исчезает, если концентрация электролитов достигает величин, при которых границы дальней гидратации ионов соприкасаются. [30]
Страницы: 1 2 3