Ионная гидратация
Cтраница 2
Так как за ГПГ нет воды, не участвующей в первичном гидра-тационном процессе, и имеется ее дефицит по сравнению с требуемыми координационными числами ионной гидратации, то молекулы добавляемой воды устремляются в незаполненные гидратные оболочки, связываясь тем более прочно, чем выше концентрация. При этом следует учесть и относительную гидрофильность катиона и аниона, приводящую к перераспределению гидратной воды. Все это должно приводить к дополнительному снижению теплоемкости. [16]
В связи со сложностью рассматриваемого явления и многообразием его проявлений в свойствах растворов, большое значение приобретает дальнейшее развитие имеющихся и привлечение новых методов изучения ионной гидратации. Возможности данного метода в последние годы были существенно расширены за счет привлечения метода изотопного замещения и изучения получаемых на его основе данных по изотопным эффектам гидратации. [17]
Как известно, существование двух видов ближней гидратации ионов определяется наличием у воды явно выраженной упорядоченной структуры, состояние которой, в свою очередь, сильно отражается на ионной гидратации. [18]
В периоды вулканических извержений на субмикронную фракцию стратосферного аэрозоля может накладываться и более мелкодисперсная фракция частиц H2S04 с модальным радиусом гт-4 - 10 - 2 мкм, представляющая собой ядра фотогазохимиче-ского превращения SO2 в результате ионной гидратации. При отсутствии активной вулканической деятельности вклад тонкодисперсной фракции частиц в оптические свойства стратосферного аэрозоля невелик. [19]
Переход к комплексам, обладающим вторичной гидратной оболочкой, совершается скачкообразно, причем относящиеся к этому диапазону данные могут быть с равным успехом описаны целой последовательностью комплексов с одинаковыми константами равновесия, как это было сделано в работе Глюкауфа и Китта [85] при расчете ионной гидратации в фазе ионита. Комплексы, подобные RH ( H20) 8, следует рассматривать как результат некоторого усреднения, обеспечивающего весьма хорошее совпадение с экспериментальными данными. Что же касается комплексов с первичной гидратной оболочкой, то их существование, по-видимому, следует признать реальным. Было бы интересно установить, при каких условиях эти гидра-тированные ионные пары диссоциируют на свободные ионы. [20]
Ионная гидратация далее все слабее компенсирует разупорядочивание вводимых в раствор порций кислоты. [21]
Ясно, что такие свойства параметра ионного размера а заставляют искать другие короткодействующие взаимодействия. Эти стороны процесса ионной гидратации не учитываются параметром а, хотя при таком подходе принимается во внимание увеличение размера точечного заряда, обусловленное ассоциацией некоторых молекул воды с ионами. [22]
Обе изотермы имеют общие черты. В области разбавленных растворов доминирует электролитическая диссоциация и ионная гидратация. Однако в случае H2S04 моногидрат выражен исключительно четко, в случае HN03 картина более расплывчата, по-видимому, из-за наложения различных равновесий ( см. рис. 38, стр. Кроме того, здесь в зоне высоких концентраций кислоты явления значительно сложнее. [23]
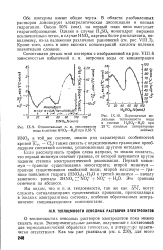 |
Относительные п. м. теплоемкости воды в системе HNO. - Н2О при 2 53 С.| Парциальные мо-ляльные теплоемкости воды в системе H2SO4 - H2O при 25 С ( сводные литературные данные. [24] |
Обе изотермы имеют общие черты. В области разбавленных растворов доминирует электролитическая диссоциация и ионная гидратация. Около 50 % ( мол), на первый план явно выступает гидратообразование. Однако в случае H2SO4 моногидрат выражен исключительно четко, в случае HNO3 картина более расплывчата, по-видимому, из-за наложения различных равновесий ( см. рис. VIII. Кроме того, здесь в зоне высоких концентраций кислоты явления значительно сложнее. [25]
 |
Частицы гекторита, окруженные частицами коллоидного кремнезема. [26] |
Эти авторы также показали, что при поглощении большего количества воды сверх единичного слоя между пластинками изменяются наклоны изотерм вследствие образования слоя между пластинками. Различия в изотермах водной десорбции объясняются на основании эффектов ионной гидратации. Количество молекул воды на один обменоспособный ион следующее: магний и кальций удерживают восемь молекул, стронций и барий - четыре молекулы, водород - три, а литий - одну, вероятно, потому, что литий удерживается другим способом. [27]
Влияние растворенных ионов на структуру воды отличается от влияния на нее нейтральных молекул. Изменения в структуре воды, вызванные ионами, невозможно отделить от явления ионной гидратации ( см. разд. Тем самым электрическое тюле ионов разрушает и размягчает области с льдоподобной структурой в отличие от влияния нейтральных молекул, которые стабилизируют первичную структуру воды. [28]
Важные соотношения между электроотрицательностыо и энергией решеток: возможность оценки так называемых термохимических ионных радиусов на основе термохимических измерений, разработанная А. Ф. Капу-стинским совместно с К. Б. Яцимирским; интересные эмпирические связи между энтропиями и теплоемкостями отдельных ионов, с одной стороны, и их радиусами, с другой, - лот далеко неполный перечень результатов этих работ, пополнивших арсенал фактов и выводов, способствующих дальнейшему развитию теории растворов. Ряд статей А. Ф. Капустинского посвящен также центральной проблеме теории растворов электролитов - проблеме ионной гидратации. [29]
Важные соотношения между электроотрицательностью и энергией решеток; возможность оценки так называемых термохимических ионных радиусов на основе термохимических измерений, разработанная А. Ф. Капу-стинским совместно с К. Б. Яцимирским; интересные эмпирические связи между энтропиями и теплоемкостями отдельных ионов, с одной стороны, и их радиусами, с другой, - вот далеко неполный перечень результатов этих работ, пополнивших арсенал фактов и выводов, способствующих дальнейшему развитию теории растворов. Ряд статей А. Ф. Капустинского посвящен также центральной проблеме теории растворов электролитов - проблеме ионной гидратации. [30]
Страницы: 1 2 3