Гидрофобная гидратация
Cтраница 2
В целом, приведенные данные еще раз демонстрируют определяющую роль гидрофобной гидратации в формировании отрицательного начального хода объемного эффекта смешения при добавлении неэлектролитов к воде. Причина bv О для раствора ацетонитрила обсуждается ниже, в связи с рассмотрением концентрационной зависимости Фу2 ( я) Для некоторых систем. [16]
В присутствии инертных растворенных веществ, например алифатических углеводородов, вода подвергается гидрофобной гидратации, проявляющейся в образовании зоны плавающих айсбергов. Фрэнк и Эванс [143] приписали это неожиданное явление взаимодействию типа масло на взбитой воде, при котором слабая поляризуемость инертного растворенного вещества приводит к неспособности передавать воздействия, приводящие к разрушению кластеров. Вследствие этого воздействие на кластеры локально смягчается. В свою очередь, кластеры, находящиеся в зоне такого смягченного воздействия, обеспечивают защиту поверхности льдоподобных кластеров, соседних с ними. То, что многообразие противоположных химических воздействий может привести к синергизму в повышении упорядоченности, которая, в свою очередь, может затем возрасти при воздействии пространственно упорядоченной матрицы, включающей, например, полости между регулярно расположенными кристаллитами равных размеров, согласуется с образованием дальнего порядка и иммобилизацией воды внутри мембраны и у границы раздела мембрана - раствор. [18]
Изменение в объеме при мицеллообразовании обычно положительно [45], что также приписывается уменьшению гидрофобной гидратации ( гл. [19]
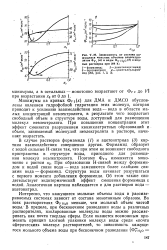 |
Зависимость от состава кажущихся мольных объемов неэлектролитов Фу2 ( а и воды Фу pj2o ( в водных растворах при 298 К. [20] |
Минимумы на кривых vz ( x) Для ДМА и ДМСО обусловлены явлением гидрофобной гидратации этих молекул, которая приводит к усилению взаимодействия вода - вода в области малых концентраций неэлектролита, в результате чего возрастает свободный объем в структуре воды, доступный для размещения молекул неэлектролита. При повышении концентрации этот эффект сменяется разрушением квазиклатратных образований и объем, занимаемый молекулой неэлектролита в растворе, начинает возрастать. [21]
Денуайе, Пеллетье и Жоликер [224] показали, что такое всаливание связано с гидрофобной гидратацией вблизи этих солей. Растворимость неполярных электролитов в значительной степени лимитируется возрастанием энтропии, которое происходит вследствие упорядочения структуры воды при их растворении. Крупные гидрофобные ионы также вызывают упорядочение структуры воды. Обладая более упорядоченной структурой, чем чистая вода, растворы указанных солей требуют меньшей работы для растворения неэлектролита, вследствие чего растворимость последних возрастает. Растворение мылами и моющими средствами представляет предельные случаи всаливания. При этом образуется смешанная мицелла из неэлектролитов и органических ионов с длинной цепью. Рассмотренная Немети и Ше-рагой [75] гидрофобная связь и предположенное Диамондом [225] спаривание образующих структуру ионов также можно считать связанными с всаливанием. [22]
Данные температуры являются предельными, при которых на зависимостях Csm f ( X2) проявляется эффект гидрофобной гидратации. [23]
Таким образом, машинный эксперимент позволяет сделать однозначный вывод, что полярные группы не способны помешать гидрофобной гидратации. Это, в свою очередь, означает, что g21 имеет сложную угловую зависимость. В менее наглядном виде это значит, по причине, отмеченной выше, что функция ш22 сложным образом зависит от взаимной ориентации молекул L. Подход к этой и связанной с ней проблемой расчета термодинамических свойств находится пока на самой начальной стадии разработки. [24]
С - 2 особенно резко, когда их два и более, при наличии же одной полярной группы доминирует гидрофобная гидратация. [25]
С другой стороны, в воде, где для органических молекул, содержащих неполярные группы, важную роль играет гидрофобная гидратация, возможны аналогичные эффекты и для крупных органических ионов, в которых заряд делокализован по большому объему. [26]
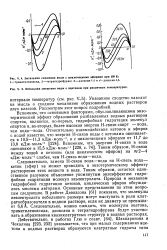 |
Энтальпии смешения воды с циклическими эфирами при 298 К.| Энтальпии смешения воды с ацетоном при различных температурах. [27] |
Вспомним, что основными факторами, обуславливающими экзотермический эффект образования разбавленных водных растворов спиртов, являются, во-первых, гидрофобная гидратация молекул спиртов и, во-вторых, более высокая энергия Н - связи спирт - вода, чем вода-вода. Вспомним, что энергию Н - связи в воде оценивают в 15 5 кДж - моль - [ 228, с. Таким образом, Н - связи между водой и кетоном ( или циклическим эфиром) на 2 - 4 кДж - моль 1 слабее, чем Н - связь вода-вода. [28]
 |
Сводная энергия, энтальпия и энтропия образования мицелл в воде при 25 С. [29] |
Движущая сила мицеллярной агрегации обычно исходит из доминирующих положительных энтропийных вкладов ( табл. 3.11), отождествляемых с нарушением гидрофобной гидратации ( гл. [30]
Страницы: 1 2 3 4 5
