Гидрофобная гидратация
Cтраница 4
В случае третичных алкилгалогенидов в воде при комнатной температуре типичными значениями Д5 ДС и & г / n п являются 5 - 20 энтр. Это явление более четко описывается как замена гидрофобной гидратации на уровне реагентов отрицательной гидратацией в переходном состоянии. Процесс активации фактически является полным аналогом умозрительного процесса, описанного в разд. Процесс сопровождается потерей энтропии и большой положительной теплоемкостью, характерными для гидрофобной гидратации, отсюда наблюдаемые знаки акти-вационных параметров. [46]
Как ясно из предыдущего, по экспериментальным термодинамическим данным очень легко отличить монофункциональные гидрофобные частицы L от монофункциональных гидрофильных. Именно опыт и привел к эмпирическим определениям понятий гидрофобной гидратации и гидрофобного взаимодействия. В литературе неоднократно публиковались сводки свойств растворов, характерных для гидрофобного и негидрофобного поведения растворенных веществ ( см. [7, 12, 55, 56]), которые очень хорошо помогают для выявления полярно противоположных случаев. [47]
 |
Потери массы силиката ЧА ( SiO2 / NR412 5 в зависимости от температуры и времени сушки Числа у кривых - время сушки в минутах.| Время гелеобразования раствора силиката ЧА ( SiO2 / NR4 12 5 при. [48] |
Различные виды гидратации положительных и отрицательных частиц в растворах полисиликатов ЧА резко изменяют поляризационные свойства дисперсной фазы и обусловливают ее высокую УСТОЙЧИВОСТЬ к ассоциативным процессам. Известно [22], что для ионов четвертичного аммония характерна сильная гидрофобная гидратация, приводящая уже у ТБА к образованию клатратных структур и частиц, в противоположность положительной гидрата - Чии кремнезема. В целом это сочетание обусловливает низкую поляризуемость дисперсных частиц и тем самым высокую стабильность системы. [49]
Следовательно, замена Н - связи вода-вода на Н - связь вода - кетон ( эфир) не может приводить к экзотермическому эффекту растворения этих веществ в воде. Таким образом, остается единственное разумное объяснение упомянутым экзоэффектам: гидрофобная гидратация молекул неэлектролита. [50]
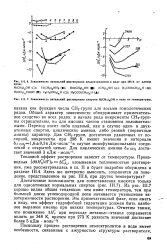 |
Зависимость энтальпий растворения спиртов Н ( СН2 ОН в воде от температуры. [51] |
Из рис. III.7 хорошо видна общая тенденция: чем ниже температура, тем при большей длине углеводородной цепи начинается уменьшение эк-зотермичности растворения. Это примечательный факт, если иметь в виду, что эффект гидрофобной гидратации должен быть наиболее выражен именно при низких температурах. [52]
VJ ( xz) для систем, приведенных выше, позволяет рассматривать парциальный мольный объем неэлектролита в растворе, в качестве структурно-чувствительного свойства. II ] отметим еще раз, что dVz / dxz 0 свидетельствует о явлении гидрофобной гидратации, которая приводит к упрочнению связей вода - вода в окрестности растворенной частицы неэлектролита. Усиление структурной организации воды в области 0 х2 xl подтверждается несколькими независимыми методами. [53]
 |
Относительное изменение скорости ультразвука в водных растворах солей. [54] |
С - концентрация растворенного вещества; А и В - постоянные. Используя эти зависимости, Хорн показал, что наряду с кулоновской гидратацией ионов существует и гидрофобная гидратация молекул неполярных или гидрофобных веществ, а также присутствующих в растворе молекул газов. Сущность ее основана на окружении этих молекул клеткоподобной или клат-ратной гидратационной атмосферой. [55]
Оказалось, что зависимости Csm f ( X2) в данных системах при 273 - 283 К, так же как и в водных растворах метанола, имеют экстремальный характер. Однако максимальные значения растворимости газов смещаются в область меньших концентраций спиртов в последовательности этанол - изопропанол-н-пропанол, что связано с усилением эффекта гидрофобной гидратации с увеличением эффективных размеров молекул спиртов в этом ряду. [56]
В соответствии с концепцией О.Я. Самойлова [15] о наименьшем возможном изменении структуры воды при образовании раствора структура разбавленного водного раствора электролита может рассматриваться как структура воды, измененная присутствием гидрагирующихся ионов. При этом доля собственной структуры воды в растворе по сравнению с чистой водой всегда ниже, независимо от вида гидратации ионов ( за исключением случая гидрофобной гидратации), хотя, в отдельных случаях ( положительная гидратация) общая упорядоченность раствора может быть выше, чем у растворителя. [57]
Оказалось, что сопровождающие их гидратацию эффекты ( термодинамические, кинетические, изотопные и др.) настолько отличаются от эффектов ионной гидратации, что это привело к появлению понятия о гидратации второго рода или гидрофобной гидратации. [58]
К ним относятся поляризация молекул воды в поле иона ( сдвиг в слабое поле для С и А -), перераспределение зарядов в связи О - Н вследствие взаимодействия с окружающими поляризуемыми ионами ( низкопольный сдвиг), разрыв водородных связей ( высокопольный сдвиг), образование водородных связей в результате гидрофобной гидратации ( сдвиг в слабое поле) и ассоциация ионов. Значение факторов, индуцирующих разрыв связей, выявляется при сравнении с аналогичными эффектами в жидком аммиаке, в котором все сдвиги, во-первых, низкопольные, во-вторых, зависят главным образом от катионов и, в-третьих, возрастают при уменьшении радиусов ионов [16], Именно таково ожидаемое поведение, обусловленное поляризационным вкладом, который в случае воды должен быть сходным. Поскольку а имеет преимущественно положительные значения, отсюда следует, что процент разрыва водородных связей большой. Рост положительного значения а с ионным радиусом означает отрицательную гидратацию. Высокопольный сдвиг, индуцированный катионами R4N - t -, которые по данным многих других методов представляют собой центры сильной гидрофобной гидратации ( т.е. усиление образования водородных связей), и низкопольные сдвиги до сих пор могут быть объяснены согласно теории гидрофобных веществ в водных растворах. В следующем разделе предлагаются возможные объяснения этих эффектов. [59]
Действие иона на тепловое и трансляционное движение ближайших молекул можно разделить на две составляющие. Первая ( гидрофильная гидратация) связана с наличием положительной или отрицательной гидратации, она растет с повышением температуры и уменьшается при переходе от растворов в обычной воде к растворам в тяжелой воде. Вторая ( гидрофобная гидратация) характеризуется тем, что часть растворенного вещества оказывает на трансляционное движение молекул тормозящее действие и вызвана тем, что часть пространства раствора, соответствующая собственному объему частиц растворенного вещества, оказывается недоступной для молекул воды. Эта составляющая растет с увеличением размера частиц растворенного вещества. [60]
Страницы: 1 2 3 4 5