Гидрофобная гидратация
Cтраница 3
Указанные факты говорят о том, что стабилизация структуры воды вблизи растворенных атомов благородного газа происходит не столько за счет усиления водородных связей вблизи растворенных частиц ( гидрофобная гидратация), сколько за счет увеличения доли участков упорядоченной структуры, где молекулы воды связаны сильными тетраэдрическими водородными связями. [31]
Судя по проводимости ионов тетралкиламмония в HgO и D2O, их радиусы по Стоксу одинаковы [176], из чего можно заключить, что в этих растворах происходит гидрофобная гидратация, включающая образование решетчатых структур. [32]
Оказалось, что и в этом случае зависимости Csm / ( Тг) при 273 - 283 К проходят через максимум, т.е. проявляются эффекты, подобные гидрофобной гидратации. [33]
Приведенные результаты показывают, что гидрофобная гидратация в отличие от гидрофильной существенно зависит от структурного состояния воды: чем больше стабилизирована собственная структура воды, тем сильнее выражен эффект гидрофобной гидратации. Все другие типы упорядочивания уменьшают этот вид гидратации. [34]
Однако проведенные расчеты [2] показали, что гипотетическая нейтральная частица, используемая в качестве модели состояния иона в растворе, не полностью адекватна изоэлектронному атому благородного газа и не обладает способностью к гидрофобной гидратации. [35]
Пониженная подвижность R4 N по сравнению с ожидаемой по закону Стокса в водных растворах, если сопоставлять их со спиртовыми растворами тех же солей и полагать, что спиртовые растворы подчиняются закону Стокса с нормальными сток-совыми радиусами, также указывает на повышение локальной вязкости в результате гидрофобной гидратации ( разд. [36]
 |
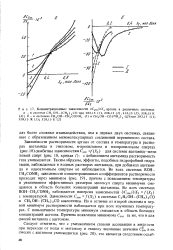
Положение и относительная глубина минимумов VJ некоторых одноатомных и двухатомных спиртов. [37] |
Образование последней происходит вследствие гидрофобной гидратации, обусловленной наличием неполярных групп в молекуле неэлектролита. Диаметр зоны гидрофобной гидратации возрастает с ростом размера неполярной части молекулы неэлектролита. [38]
Отметим, что все без исключения энтальпии растворения, полученные в [114, 115] - эндотермические. Таким образом, гидрофобная гидратация резко выделяет воду среди всех растворителей в отношении растворения неполярных молекул и групп, как это уже обсуждалось выше в этом разделе, а также в гл. [39]
До сих пор мы умышленно избегали термина гидрофобная гидратация, поскольку в литературе он, а также термин Гидрофобное взаимодействие трактуются очень по-разному. В дальнейшем под гидрофобной гидратацией мы подразумеваем всю совокупность особенностей взаимодействий с водой неполярных молекул и групп в бесконечно разбавленном растворе. В отличие от этого гидрофобное взаимодействие проявляется в растворах конечных концентраций, когда возникают вклады в термодинамические функции от взаимодействия неполярных молекул друг с другом. [40]
Как ожидается для этой модели, Д5, ДС и их отношение зависят от структуры субстрата. Это согласуется с уменьшением гидрофобной гидратации исходного состояния из-за присутствия групп, способных к образованию водородных связей ( см. разд. [41]
Для получения абсолютных значений F галогенидных ионов использование галогенидов тетралкиламмония дает возможность применить другой метод. Вблизи больших катионов тетралкиламмония происходит гидрофобная гидратация, которую в первом приближении можно, по-видимому, принять пропорциональной размеру этих ионов. В то же время вблизи указанных больших катионов не возникает гидрофильная и, следовательно, отрицательная гидратация. [42]
Зависимости растворимости аргона от состава и температуры в растворах ацетамида в этиловом, - пропиловом и изопропиловом спиртах ( рис. 18) симбатны зависимостямCsm f ( X2) для системы ацетамид-метиловый спирт ( рис. 18, кривая 1): с добавлением ацетамида растворимость газа уменьшается. Таким образом, эффекты, подобные гидрофобной гидратации, наблюдаемые в водных растворах ацетамида, при добавках ацетамида к одноатомным спиртам не наблюдаются. Во всех системах R0H - CH3CONH2 зависимости концентрационных коэффициентов растворимости проходят через минимум ( рис 19), причем с повышением температуры и увеличением эффективных размеров молекул спирта минимумы смещаются в область больших концентраций ацетамида. Во всех системах ROH - CH3CONH2 наблюдается инверсия зависимостей dCsm / dX2 / №) с температурой. Зависимости Csm f ( X2) в системах С2Н5 ОН - ( СН3) 2 СО и СН3ОН - ( СН3) 2СО аналогичны. Но в отличие от второй системы в первой минимум растворимости наблюдается при всех изученных температурах. С повышением температуры минимум смещается в область больших концентраций ацетона. [44]
АЯ и ГД5 несколько больше ( но все еще меньше 1 ккал / моль) и обычно совпадают по знаку ( разд. Они отрицательны, если преобладает положительная или гидрофобная гидратация, и положительны, если преобладает отрицательная гидратация. Для окси - анионов, ионов щелочных металлов и катионов R4N ДЯг г составляет около 5 %, а для галогенид-ионов - около 15 % от структурного вклада в ДЯ. [45]
Страницы: 1 2 3 4 5