Положительная гидратация
Cтраница 3
Из данных таблицы следует, что между характером влияния стехиометрических смесей ионов на структуру воды и величиной Тпреа существует хорошая качественная корреляция, т.е. чем сильнее выражены разрушающие свойства данной сте-хиометрической смеси ионов, тем дальше от 273 К отстоит температурная граница ее отрицательной гидратации. Значит, предельная температура может рассматриваться как количественная мера отрицательной или положительной гидратации ионов. [31]
Влияние ионов на трансляционное движение молекул воды может по-разному зависеть от их размера, заряда, формы и некоторых других свойств. Если скорость обмена низка, подвижность молекул воды, расположенных рядом с ионом, снижается и величина положительной гидратации велика. Если, однако, обмен ускорен по сравнению с обменом между соседними молекулами в чистой воде, то происходит отрицательная гидратация. [32]
В соответствии с более ранними представлениями в водных растворах ионов, кристаллографический радиус которых меньше радиуса молекулы воды, наблюдается положительная гидратация. Как следует из некоторых физико-химических свойств, характер гидратированного иона влияет также и на молекулы воды, расположенные за пределами гидратной оболочки иона. Число молекул воды, находящихся в областях со структурой, разрушенной под влиянием ионов, также зависит от размера, заряда и электронной структуры иона. Это число может быть в 1 2 - 2 4 раза больше числа гидратации. Полученные в результате классификации результаты позволили определить максимальное число гидратации ( Лтах), которое представляет собой число всех молекул воды, претерпевших структурные изменения вследствие присутствия иона, по сравнению с первоначальным состоянием в объеме воды. Максимальные числа гидратации в зависимости от атомного номера приведены на рис. 5.11. Можно заметить, что, с одной стороны, ионы можно разделить на категории в соответствии с их зарядностью. [33]
Из сравнения этих результатов с энергией активации самодиффузии ионов было сделано заключение, что гидрофобные и карбоксильные группы приводят к положительной гидратации, тогда как сульфогруппы дают в результате отрицательную гидратацию. [34]
В то же время изменение собственной структуры растворителя может приводить к тому, что при одной температуре подвижность молекул растворителя вокруг ионов меньше, чем их подвижность в чистом растворителе, а при другой - больше. Данные о температурных зависимостях активности воды в растворах электролитов [52] и предельных температурах для соответствующей стехиометрическои смеси ионов ( температура, при которой наблюдается переход от отрицательной к положительной гидратации ионов) хорошо коррелируют. [36]
Изотермы I типа характеризуются непрерывным продолжением такого хода: дегидратация, сначала только энергетическая ( зоны а и Ь), а за ГПГ и координационная ( зона с) на всем протяжении кривой доминируют над выигрышем энергии за счет сближения ионов. Экзотермический вклад разрушения структуры воды в зоне Ъ отходит на задний план, так как к типу I относятся электролиты, упорядочивающие эту структуру в первых гидратных сферах ( положительная гидратация в терминологии О. Переход ГПГ на многих кривых отражается в нерезко выраженном увеличении наклона, очевидно, за счет перераспределения дефицитной ги-дратной воды между ионами. [37]
В соответствии с концепцией О.Я. Самойлова [15] о наименьшем возможном изменении структуры воды при образовании раствора структура разбавленного водного раствора электролита может рассматриваться как структура воды, измененная присутствием гидрагирующихся ионов. При этом доля собственной структуры воды в растворе по сравнению с чистой водой всегда ниже, независимо от вида гидратации ионов ( за исключением случая гидрофобной гидратации), хотя, в отдельных случаях ( положительная гидратация) общая упорядоченность раствора может быть выше, чем у растворителя. [38]
С ионы 1Л гидратирова-лы положительно, тогда как для ионов К характерна отрицательная гидратация. Отрицательная гидратация ионов Na, наблюдаемая при низкой температуре, становится положительной при 26 5 С. В общем повышение температуры облегчает положительную гидратацию. Гидратация иона К при температуре примерно 80 - 100 С из отрицательной становится положительной, тогда как положительная гидратация иона Li при понижении температуры от - 10 до - 15 С изменяется на отрицательную. [39]
При взаимодействии с монтмориллонитом, в котором обменные реакции на поверхности протекают быстрее и полнее, возможно получение эффекта калиевой обработки. Применяя - представления О.Я. Самойлова об отрицательной и положительной гидратации ионов, вышеуказанные авторы делают предположение о том, что проникновение катиона калия в гексагональную лунку ( средний радиус 0 165нм) слоев глинистых минералов возможно до температуры 44 С в случае применения хлористого калия. При более высокой температуре ион калия в составе КС1 характеризуется положительной гидратацией ( радиус 0 38нм), и возможность миграции гидратированного иона в глубь минерала уменьшается, так как при более высоких температурах практически нет различий между, например, гидратированными ионами калия и натрия; для них одинаково недоступны гексагональные лунки. Эффективность калиевой обработки монтмориллонита будет достигнута, если забойная температура достаточно низкая и раствор не загрязнен многовалентными катионами. Этой же точки зрения придерживаются и другие авторы. Однако эти теоретические исследования не учитывают многообразия факторов, влияющих на характер взаимодействия ионов калия и глинистого минерала, таких как щелочность среды, давление и температура, присутствие других солей. [40]
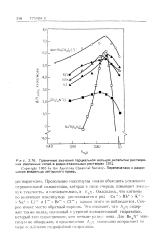 |
Граничные значения парциальной мольной энтальпии растворения различных солей в водно-этанольных растворах. [41] |
Ожидалось, что катионы по величинам максимумов расположатся в ряд Cs Rb К Na Li и 1 - Вг - С1 -; однако этого не наблюдается. Скорее имеет место обратный порядок. Это означает, что Л0т ] содержит также вклад, связанный с утратой положительной гидратации, который тем существеннее, чем меньше радже иона. Для Bn4N максимум не обнаружен, и произведение Л0г; монотонно возрастает по мере ослабления гидрофобной гидратации. [42]
Система Ba ( N03) 2 - Fe ( N03) 3 - Н20 исследована нами при 25 С. В области макросоотношений ( до 1: 100) на диаграммах растворимости всех систем имеются области кристаллизации индивидуальных компонентов. Эвтоническая точка сильно смещена в область малых концентраций нитрата бария вследствие значительного эффекта положительной гидратации катионов переходных элементов. В частности, с учетом данных [4] коэффициент, характеризующий отношение времен релаксации протонного обмена в воде и растворе соли, составляет - 0 65 для двухвалентных переходных элементов по сравнению с соответствующей величиной 0 25 для иона бария. [43]
Формы и виды распространения ОВ и УВ в земной коре определяются геохимическими и термодинамическими условиями, которые изменяются в процессе литогенеза и эволюции геогидродинамических систем. Для стадии седиментогенеза характерны низкие давление, температура и минерализация вод и преимущественно окислительные условия. Низкое давление способствует разупорядочению структуры воды [ Блох А. М., 1969 г. ], благодаря чему облегчается переход в воду ионов с положительной гидратацией ( кальция, магния, сульфат-и карбонат-ионов): известняки, гипсы, ангидриты и другие породы растворяются. Это обусловливает чрезвычайную пестроту минерализации и состава вод, среди которых преобладают хлоридные талассоген-ные и сульфатно-бикарбонатные метеогенные воды. [44]
Простые ионы, которые по значениям А5, г ( разд. В, отрицательные 1Л и времена переориентации тг, превосходящие эти величины для чистой воды. Такие ионы, следовательно, снижают вращательную и поступательную подвижность соседних молекул воды. Термодинамические и кинетические критерии в данном случае согласуются, указывая на преобладание положительной гидратации для ионов Li, F -, OH - и для большинства двух - и многозарядных ионов. Полностью ли подавляется вращение молекул воды в первичной гидратной оболочке этих ионов. Некоторые данные указывают на то, что для большин - - гва ионов этого в действительности нет. Детальный анализ [430] данных по диффузии и магнитной релаксации 19F и 1Н в водных растворах фторидов также показывает, что изменение положения одного атома Н относительно другого происходит быстрее, чем изменение положения Н относительно F. Наконец, времена диэлектрической релаксации т, хотя и не коррелируют точно с тг, в присутствии любых ионов уменьшаются. Можно предположить, что положительно гидратированные ионы полностью иммобилизуют молекулы воды в первой координационной оболочке по тем степеням свободы, которые определяют ориентационный вклад в диэлектрическую проницаемость. Следовательно, т относятся к более удаленным молекулам воды, которые участвуют в отрицательной гидратации. [45]
Страницы: 1 2 3 4