Гидрид - кальций
Cтраница 2
Гидрид кальция СаН2 - очень эффективный осушающий реагент. Его реакция с водой протекает необратимо в широком интервале температур. [16]
Гидрид кальция, по свидетельству А. Г. Елицура, в сравнении с другими гидридами наиболее удобен по легкости хранения, обращению с ним и спокойному течению реакции. [17]
Гидрид кальция горит в воздухе, а с водой взаи-модействует с выделением водорода. [18]
Гидрид кальция получают действием сухого водорода на кальций в пределах температур 400 - 600 С. При температурах выше 800 С гидрид разлагается с образованием кальция и водорода. Образующийся атомарный водород тотчас же соединяется в молекулы водорода. При 970 С равновесное давление водорода над гидридом достигает 1 ат. [19]
Гидрид кальция получается при действии сухого и чистого водорода на кальций при температуре 400 - 600 С. [20]
Гидрид кальция ( гидролит), СаН2, обнаружен спектральным методом на Солнце и звездах. Его получают, сжигая металлический кальций в чистом водороде. [21]
Гидрид кальция применяют для получения, осушки и очистки водорода, в аналитической химии ( определение следов воды в органических растворителях - бензоле, толуоле, четыреххлористом углероде), в производстве металлов - титана, циркония, ванадия, ниобия, тантала, урана и других путем восстановления их окислов, а также для получения гидрида лития или двойного кальцийалюми-нийгидрида и в черной металлургии, где с помощью СаН2 удаляют серу из стали и раскисляют хром. [22]
Гидрид кальция был приготовлен действием водорода на нагретый докрасна кальций, помещенный в никелевую лодочку, а также пропусканием водорода через расплавленный кальций. Сведения об устойчивости гидрида кальция СаН2 противоречивы. Так, по данным одних исследователей гидрид кальция не способен диссоциировать при температуре до 600, по данным же других исследователей - диссоциация гидрида кальция при этой температуре становится уже заметной и быстро возрастает с повышением температуры. [23]
Гидрид кальция устойчив при нагревании. [24]
Гидрид кальция должен находиться вне печи, но настолько близко к ее нагретой части, чтобы выделяющиеся водяные пары не могли остыть и сконденсироваться на стенках сосуда. [25]
 |
Сосуд Ландольта. [26] |
Гидрид кальция вносится в реакционный сосуд следующим образом: сначала туда помещаются пробирка с навеской и стерженек, за ними вставляется укрепленный на проволоке тампон из прокаленного асбестового волокна и, наконец, на тампон насыпается гидрид кальция. Тампон позволяет легко вынимать смесь гидрида и гидроокиси кальция и предохраняет от попадания гидрида кальция в глубь реакционного сосуда. [27]
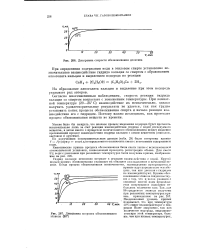 |
Диаграмма скорости обезвоживания диоксана.| Диаграмма скорости обезвоживания этанола ( 96. [28] |
Гидрид кальция мгновенно вступает в реакцию взаимодействия с водой. Крутой подъем кривых обезвоживания указывает на обильное газовыделеппе в начальный момент. [29]
Гидрид кальция помещается в холодной части реакционной пробирки, выходящей из печи. Активированный уголь помещается в трубку небольшого диаметра, которая присоединяется к реакционной пробирке. [30]
Страницы: 1 2 3 4