Гидрид - переходный металл
Cтраница 1
Гидриды переходных металлов, такие как гидриды титана, циркония, ванадия, ниобия и другие, получают восстановлением их окислов металлическим кальцием, магнием либо их гидридами. Основным восстанавливающим агентом является металл, поддерживаемый при реакции в парообразном состоянии; водород усиливает процесс восстановления и предотвращает окисление продукта. Процесс проводится при температурах около 1000 - 1100 С в аппаратуре, выполненной из нержавеющей стали. Полученный гидрид отмывают от окислов слабыми растворами кислот. [1]
Гидрид переходного металла может быть необходим для изомеризации олефина, однако не все гидриды переходных металлов активны. [2]
Гидриды переходных металлов в основном гидрируются насквозь; поэтому выход продукта всегда 100 %, однако состав продукта не всегда достигает стехиометрии. [3]
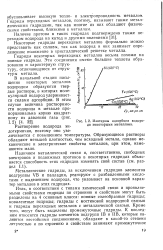 |
Изотермы адсорбции водорода некоторыми металлами. [4] |
Гидриды переходных металлов, поэтому, называют также металлическими гидридами, так как многие из них обладают физическими свойствами, близкими к металлам. [5]
Гидриды переходных металлов играют решающую роль в гомогенно-каталитических реакциях изомеризации олефинов. В качестве катализаторов могут быть использованы истинные гидриды, такие, как НСо ( СО) 4, или комплексы переходных металлов со стабилизирующими лигандами; во многих случаях каталитические реакции почти наверняка протекают через промежуточные гидриды. [6]
Гидриды переходных металлов, или так называемые металлические гидриды, обязаны последним своим названием тому что они, как и метал-лиды, часто имеют нестехиометрический состав. [7]
Гидриды переходных металлов по внешнему виду и некоторым свойствам подобны металлам. Характер химической связи в этих гидридах близок к металлической. Они также обладают восстановительными свойствами, но менее активны, чем ионные гидриды. Большинство из них с водой взаимодействует слабо. [8]
Гидриды переходных металлов, проявляющие активность в реакции переноса водорода и катализе, например 1 - 9, обычно содержат такие стабилизующие лиганды, как фосфин, карбонил, цианид или л-цикло-пентадиенил, способные к ретродативному л-связы-ванию. [9]
 |
Классификация гидридов. [10] |
Гидриды переходных металлов очень разнообразны по своим свойствам. Многие из них образуются при прямом действии водорода на металлы. Лучше всего изучены и наиболее важны гидриды, образуемые лантаноидами, актиноидами, а также элементами IVA и VA групп. [11]
Гидриды переходных металлов являются весьма интересным классом неорганических соединений. Глубокое изучение гидридов открывает новые возможности понимания химической природы фаз переменного состава. [12]
Гидриды переходных металлов, несмотря на то, что их изучение интенсивно проводилось только за последние 10 - 15 лет, имеют интересные направления практического применения; далеко еще не все их возможности используются в современной технике. [13]
Гидриды переходных металлов в вакууме начинают разлагаться при очень низких температурах. Тригидриды редкоземельных металлов разлагаются в области 250 - 300 С, гидриды металлов IV и V групп периодической системы - в области 300 - 400 С, гидриды металлов VI и VIII групп неустойчивы уже при комнатной температуре. К последним относится группа промежуточных гидридов с частично ковалентным типом связи - гидриды цинка, меди, алюминия. В основном они уже неустойчивы при комнатной температуре и только некоторые могут сохраняться до температуры 90 - 120 С. [14]
Гидриды переходных металлов более инертны по отношению к воде и водным растворам кислот. Только гидриды редкоземельных металлов гидролизуются водой, остальные гидриды к воде н водяным парам относительно устойчивы. С кислотами гидриды металлов IV-VIII групп реагируют в очень жестких условиях - при большой концентрации кислоты и нагревании. Плавиковая кислота разлагает все гидриды. [15]
Страницы: 1 2 3 4