Гидрид - переходный металл
Cтраница 2
Термически устойчивые гидриды переходных металлов обладают кинетической стабильностью и обычно подчиняются правилу 18злектронов, за исключением плоских квадратных комплексов платины ( II), где металл имеет 16 электронов. [16]
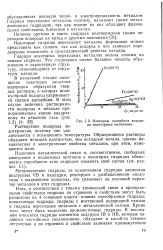 |
Изотермы адсорбции водорода некоторыми металлами. [17] |
Некоторые гидриды переходных металлов формально можно представить как сплавы, так как водород в них занимает определенное положение в кристаллической решетке металла. [18]
Многие гидриды переходных металлов чувствительны к присутствию кислорода. Следовые количества кислорода могут инициировать радикально-цепное замещение, тогда как в более высоких концентрациях кислород выступает как ингибитор. [19]
Если гидриды переходных металлов находятся в дейтерированных протонных растворителях, часто происходит дейтериевый изотопный обмен. [20]
Образование гидрида переходного металла в результате прото-нирования может оказать весьма существенное влияние на свойства исходных лигандов. [21]
Роль гидридов переходных металлов в каталитических реакциях диенов лучше всего видна на примере синтеза гексадиенов. [22]
Реакции гидридов переходных металлов с алкинами широко не изучались. Реакция HRhCl2L2 [ L P ( C6Hs) 3 ] с ацетиленом, по-видимому, является единственным описанным случаем присоединения гидрида металла к ацетилену с образованием надежно идентифицированного винильного комплекса. Однако реакции замещенных ацетиленов с гидридами хорошо известны. [23]
Применение гидридов переходных металлов облегчает синтез их силицидов. Реакции образования силицидов этих металлов обычно экзотермические. Для получения чистых силицидов не - обходимо синтезировать их в атмосфере нейтрального газа ( обычно в аргоне) или в вакууме. С углеродом и окислами силициды реагируют медленно. [24]
Свойства гидридов переходных металлов в последнее время привлекают внимание многих исследователей как с теоретической, так и с практической точки зрения. [25]
В гидридах переходных металлов, включая лантаноиды и актиноиды, атом водорода проявляет большое многообразие в характере связи и может находиться в виде свободного атома и протона, а в некоторых случаях в виде отрицательного иона. [26]
Михеева, Гидриды переходных металлов, Изд. [27]
Переменность состава гидридов переходных металлов показывает как бы непрерывный переход в периодической системе элементов от определенных соединений через неопределенные снова к определенным. Аналогичный процесс наблюдается и в интерметаллических фазах бертоллидного и дальтоНидного типов. Здесь понятие о химической индивидуальности веществ как бы стирается и на Первый план выступает непрерывность перехода одних структур в другие при естественном сохранении атомной дискретности. А это возможно лишь при различных проявлениях сил ( полновалентных и неполновалентных) химической связи, обусловливающих образование химического соединения. [28]
При получении гидридов переходных металлов любыми методами необходимо считаться с явлениями наложения процессов адсорбции и механического включения водорода. [29]
При рассмотрении гидридов переходных металлов, следуя расположению их по периодам и группам таблицы Д. И. Менделеева, мы видим, что их свойства и состав подчиняются закономерностям, вытекающим из периодического закона. В то же время при взаимодействии с водородом выявляются индивидуальные свойства отдельных металлов. [30]
Страницы: 1 2 3 4