Гидрид - ниобий
Cтраница 1
Гидрид ниобия, NbH, получают нагреванием металлического ниобия ( в виде порошка) в атмосфере водорода, действием воды на сплав ниобий - натрий, восстановлением NbOCl3 водородом. [1]
Гидрид ниобия представляет собой серовато-черный порошок с плотностью 6 - 6 6 г / см3; он плохо растворяется в НС1, НХ03, разб. [2]
Гидрид ниобия имеет удельный вес 6 0 - 6 6; удельная теплоемкость его между 0 и 100 равна 0 0987, а между 0 и 400 5 - - 0 0834 кал / г - С. [3]
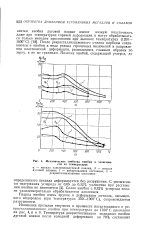 |
Механические свойства ниобия в зависимости от температуры. [4] |
Гидрид ниобия очень хрупок и деформация металла, насыщенного водородом ( при температурах 350 - 1000 С), сопровождается разрушением. [5]
Проще всего гидрид ниобия получается непосредственным гидрированием молекулярным водородом при повышенной температуре. В то же время есть указание, что компактный ниобий водород поглощает не сразу, и требуется кратковременное нагревание ниобия в атмосфере водорода с последующим охлаждением до комнатной температуры, чтобы перевести металл в активное состояние. [6]
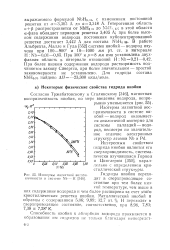 |
Изотермы магнитной восприимчивости в системе Nb - Н. [7] |
Интересным свойством гидрида ниобия является его сверхпроводимость, систематически изучавшаяся Горном и Цинглером [350], параллельно с определением кристаллической структуры. [8]
При обычной температуре гидрид ниобия устойчив на воздухе, но при нагревании переходит в пятио кись. Гидрид ниобия - NbH при температуре 15 К приобретает сверхпроводимость. [9]
Авторы предполагают, что гидриды ниобия образуются за счет восстановления ниобия атомным водородом, образующимся при реакции HF с металлическим ниобием или низшим его гидридом. [10]
Едва ли не самым интересным в химии гидридов ниобия является открытие Брауэром и Мюллером [112] гидридов ниобия в продуктах взаимодействия 10 % раствора плавиковой кислоты и металлического ниобия в водной среде. По данным рентгеновского анализа, в черном порошке, образующемся при этом, существуют две самостоятельные гидридные фазы: NbHo. Если же раствором плавиковой кислоты обрабатывается препарат состава NbH08e, то получается в индивидуальном состоянии дигидрид ниобия NbH2, причем его решетка аналогична решеткам дигидридов лантаноидов и металлов подгруппы титана. [11]
Патентные методы получения ТаНо5 - о в описаны при получения гидридов ниобия ( см. стр. [12]
Помимо поглощения водорода, при нагревании ниобия в среде водорода образуется гидрид ниобия состава NbH. Это соединение принадлежит к числу так называемых металлообразных гидридов. При нагревании в высоком вакууме до 1000 - 1200 гидрид разлагается с удалением водорода. При нагревании на воздухе гидрид легко сгорает, образуя пятиокись ниобия и пары воды. [13]
Трифторид ниобия состава NbF3 был получен Эрлихом и др. [200] реакцией гидрида ниобия со смесью водорода и фтористого водорода при 560 - 580 С. Однако Шефер и др. [9] считают, что получить NbF3 в чистом виде можно только как исключение и лишь в виде нестабильного соединения, причем не ясно, какие для этого требуются условия. Это соединение стабилизируется следами кислорода в решетке. [14]
Едва ли не самым интересным в химии гидридов ниобия является открытие Брауэром и Мюллером [112] гидридов ниобия в продуктах взаимодействия 10 % раствора плавиковой кислоты и металлического ниобия в водной среде. По данным рентгеновского анализа, в черном порошке, образующемся при этом, существуют две самостоятельные гидридные фазы: NbHo. Если же раствором плавиковой кислоты обрабатывается препарат состава NbH08e, то получается в индивидуальном состоянии дигидрид ниобия NbH2, причем его решетка аналогична решеткам дигидридов лантаноидов и металлов подгруппы титана. [15]
Страницы: 1 2 3