Гидрид - ниобий
Cтраница 3
Гидриды, полученные в растворах, чаще всего имеют строго стехиометрический состав. Сарри [243], Ю. И. Алексеева и Е. И. Крылова [244], Е. И. Крылова и А. М. Ананьиной [245] этим путем получены гидриды ниобия и тантала. [31]
В то же время Мутман, Вейс и Ридельбаум [337] предполагали, что водород в гидриде ниобия связан не стехиометрически. По их данным определения окклюдированного водорода весовым методом, отношение Nb: Н колеблется от 1 до 7 4, что несомненно является завышенным результатом, так же как и данные тех же авторов об абсорбции водорода для тантала и ванадия. [32]
Ниобий относится к числу металлов, способных образовывать с водородом гидриды. Гидрид ниобия может быть получен различными методами: восстановлением водородом соединения NbOCl3; нагреванием тонкого порошка металлического ниобия при высокой температуре в атмосфере водорода. Гидрид ниобия, полученный этими способами, отвечает по составу формуле NbH и представляет собой порошок темно-серого цвета. [33]
Если при комнатной темп-ре и давлении в 1 атм ниобий чистоты 98 5 % растворяет 104 см / г, то при 900 - только 4 см3 / г. Выше 1000 ниобий практически не взаимодействует с водородом. За пределами растворимости водород образует гидрид ниобия, обладающий высокой хрупкостью. В вакууме гидриды ниобия разлагаются. Присутствие газов заметно сказывается на механич. Особенно резко влияет на св-ва ниобия кислород. [34]
Если при комнатной темп-ре и давлении в 1 атм ниобий чистоты 98 5 % растворяет 104 см3 / г, то при 900 - только 4 см3 / г. Выше 1000 ниобий практически не взаимодействует с водородом. За пределами растворимости водород образует гидрид ниобия, обладающий высокой хрупкостью. В вакууме гидриды ниобия разлагаются. Присутствие газов заметно сказывается на механич. Особенно резко влияет на св-ва ниобия кислород. [35]
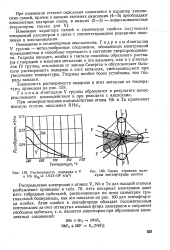 |
Растворимость водорода в V [ IMAGE ] Схема строения моле-и Nb ( Рн2 - 1 s H. MZ кулы пентафторида ниобия. [36] |
Гидриды d - металлов V группы - металлообразные соединения, обладающие электронной проводимостью и способные переходить в состояние сверхпроводимости. Гидриды ванадия, ниобия и тантала способны образовать растворы с твердыми и жидкими металлами и это вызывает, как и у d - металлов IV группы, отклонение от закона Сивертса и обусловливает большую растворимость водорода в этих металлах, уменьшающуюся при увеличении температуры. Гидриды ниобия более устойчивы, чем гидриды ванадия. [37]
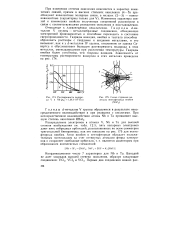 |
Растворимость водорода V и Nb ( pHi 1 013 - 105 Па.| Схема строения молекулы пентафторида ниобия ( NbF5. [38] |
Гидриды d - ме-таллов V группы - металлообразные соединения, обладающие электронной проводимостью и способные переходить в состояние сверхпроводимости. Гидриды ванадия, ниобия и тантала способны образовать растворы с твердыми и жидкими металлами, и это вызывает, как и у d - металлов IV группы, отклонение от закона Си-вертса и обусловливает большую растворимость водорода в этих металлах, уменьшающуюся при увеличении температуры. Гидриды ниобия более устойчивы, чем гидриды ванадия. [39]
 |
Растворимость водорода в V и Nb 0 н Х X 10 Па.| Схема строения молекулы пентафторида ниобия. [40] |
Гидриды d - метал-лов V группы - металлообразные соединения, обладающие электронной проводимостью и способные переходить в состояние сверхпроводимости. Гидриды ванадия, ниобия и тантала способны образовать растворы с твердыми и жидкими металлами и это вызывает, как и у d - металлов IV группы, отклонение от закона Сивертса и обусловливает большую растворимость водорода в этих металлах, уменьшающуюся при увеличении температуры. Гидриды ниобия более устойчивы, чем гидриды ванадия. [41]
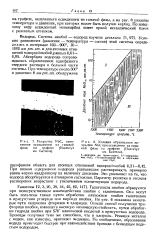 |
Условия образования покрытия NbC при осаждении из паровой фазы на графите ( Институт. [42] |
Галогениды ниобия образуются при непосредственном взаимодействии ниобия с галогенами. Они могут быть получены также путем обработки пятиокиси ниобия галогенами в присутствии углерода или карбида ниобия. На рис. 6 показаны некоторые пути получения фторидов и хлоридов. Описан способ получения три-фторпда ниобия, имеющего высокую химическую стойкость, путем обработки гидрида ниобия при 570 плавиковой кислотой в присутствии водорода. Бромиды получают теми же способами, что и хлориды. Реакция металла с иодом, как известно, протекает медленно. По сообщениям, образование иоднда происходит быстрее при взаимодействии бромида с безводным йодистым водородом. [43]
Получены и низшие йодиды ниобия. Термической диссоциацией NbJ5 был получен и NbJ4 - Корбетт и Сибо [367] получали сперва чистый NbJs непосредственным взаимодействием металла и йода ( при этом металл должен быть нагрет до 510 С, а пары йода до 180 С), а затем подвергали его диссоциации в кварцевой трубке, один конец которой был нагрет до 270 С, а другой до 35 С с тем, чтобы в нем мог конденсироваться выделяющийся йод. В таких условиях был получен серый кристаллический NbJ4, а при 430 С - черный NbJs. Тетрайодид бурно реагирует с водой и кислородом, а трийодид сходен по свойствам с трихлоридом и трибромидом. При более высокой температуре происходит образование гидрида ниобия. [44]
Страницы: 1 2 3