Гидрид - элемент
Cтраница 2
Несмотря на то что гидриды элементов главных подгрупп отнесены нами к солеобразным, возможно, что связь в некоторых или во всех этих соединениях имеет, по крайней мере частично, ковалентный характер. [16]
Неметаллические элементоорганические соединения рассматриваются как гидриды элементов, в которых некоторые или все атомы водорода замещены органическими радикалами, например ( СН3) аРН - диметилфосфин; ( CH3) 3Bi - триметилвисмутин. [17]
Из табл. 1.4 видно, что у гидридов элементов 2-го периода температуры плавления и кипения, а также теплоты испарения меньше отличаются друг от друга, чем в случае гидридов элементов 1-го периода: в наибольшей степени это относится к NH3, H20 и HF. [18]
Второй и третий методы применяются для получения гидридов элементов I - IV групп. [19]
Соединения углерода с водородом сильно отличаются от гидридов элементов VII, VI и V групп, описанных выше, как по строению, так и своим химическим поведением. [20]
Как могут быть классифицированы по строению и свойствам гидриды элементов Периодической системы. [21]
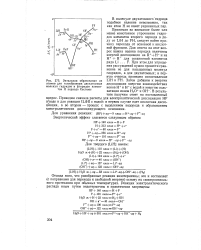 |
Энтальпии образования из атомов для газообразных двухатомных молекул гидридов и фторидов элементов II периода Системы. [22] |
Принимая во внимание более или менее монотонное упрочнение гидридов элементов второго периода в ряду от LiH до FH, следует найти причину перехода от основной к кислотной функции. [23]
Известно сравнительно мало примеров взаимодействия литийоргани-ческих соединений с гидридами элементов. Реакции в том и в другом случае осуществляются лишь постепенно и обычно выделяются смеси соединений. [24]
Так, восстановительная способность комплексов гидрида лития с гидридами элементов главной подгруппы III группы периодической системы возрастает при переходе от бора к алюминию и уменьшается при переходе от алюминия к таллию. [25]
Многообразие типов связи, резкий переход в строении и свойствах гидридов элементов при переходе от одной к другой соседней основной подгруппе периодической системы, не могут быть полностью объяснены современными взглядами на химическую связь и требуют дальнейшего ее развития. [26]
Реакции совместного распада двух и более МОС или МОС с гидридом элемента в последнее время приобретают широчайшее применение в электронике для синтеза и эпитаксиалыюго выращивания соединений типа AnBm. Доказано [31, 39], что степень загрязнения пленок углеродом сравнительно не велика, и они могут с успехом применяться в электропике. [27]
 |
Названия родоначальных гидридов. [28] |
В элементорганических соединениях в качестве родоначального соединения часто можно принять либо гидрид элемента, либо органическое соединение. Это приводит к существенно различающимся названиям. В СА органическую часть считают родона-чальной, если она содержит любую функциональную группу, называемую в суффиксе. [29]
Кажется весьма вероятным, что теория Хунда-Мулликена более применима к рассмотрению гидридов элементов. Это связано с малым размером протона и с тем, что расстояние между ним и тем атомом, с которым он соединен ( получаемое из спектроскопических данных), настолько мало, что можно считать, что протон находится внутри оболочки валентных электронов, которая только слегка деформируется. Следовательно, можно сказать, что каждый протон участвует в образовании всей валентной оболочки. Как мы уже видели, эта теория также оказывается полезной при рассмотрении двухатомных молекул легких элементов. [30]
Страницы: 1 2 3 4