Гидрид - элемент
Cтраница 4
Гидриды лантаноидов и актиноидов имеют, по-видимому, преимущественно ионную природу, но еще не удалось создать вполне удовлетворительное описание их строения. Гидриды элементов IVA и VA групп еще менее изучены. [46]
В жидкой воде атом кислорода окружен четырьмя соседними атомами, поэтому водородные связи здесь слабее ( 5 ккал / молъ); еще слабее они в жидком аммиаке. Гидриды элементов следующего периода РН3, H2S и НС1 не проявляют тенденции к образованию водородных связей. Это следует из сравнения их температур замерзания и кипения. [47]
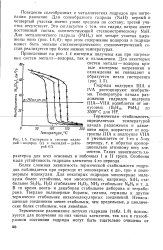 |
Гистерезис в системе палла. [48] |
Такая зависимость характерна для всех основных и побочных I и II групп. Особенно мала устойчивость гидридов элементов 4-го периода. [49]
Водородные связи между молекулами воды объясняют аномалию в температурах кипения гидридов. Так, у гидридов элементов 6 - й группы от Н2Те к H2S температура кипения понижается, и только у Н2О она резко повышена благодаря ассоциации ее молекул через Н - связи. Аналогичную аномалию проявляет NH3 в пятой и HF в седьмой группе элементов. [50]
Присоединение гидрида к ненасыщенной углерод-углеродной связи напоминает описанные выше реакции ( галогенид металла и олефин, стр. Далее, с гидридами элементов, обладающих не очень сильными акцепторными свойствами, такими, как кремний, степень полимеризации при взаимодействии с простыми алифатическими олефинами невелика и с хорошим выходом образуются производные нормальных алкилов. [51]
Примерное представление об энергии водородной связи во льду можно получить из теплоты сублимации - энергии, необходимой для превращения одного моля молекул из твердого состояния в газообразное. В табл. 8.5 сравниваются теплоты сублимации гидридов элементов IV и VI групп. Ни одна из этих молекул He-образует водородных связей. [52]
В химическом отношении элементы первого большого периода - железо, кобальт и никель - несколько отличаются от шести так называемых платиновых металлов. Это различие проявляется и в химии гидридов элементов семейства железа, с одной стороны, и платины - с другой. [53]
Название металлорганического соединения складывается из названия радикала, связанного с металлом, и названия металла, например, СН3 - Na-метилнатрий, ( C2H5) 2Hg - диэти л-ртуть, C2H5MgBr - бромистый этилмагний. Соединения неметаллов и нехарактерных металлов рассматриваются как гидриды элементов, в которых некоторые или все атомы водорода замещены органическими радикалами, например, ( СН3) 2РН - диметилфос-фин; ( CH3) 3Bi - триметилвисмутин. [54]
Страницы: 1 2 3 4